如图为元素周期表的一部分,请参照元素①~⑨在表中的位置回答下列问题:

(1)②和③的最高价含氧酸的酸性强弱关系是H2CO3H2CO3>H3BO3H3BO3。(用化学式填写)
(2)⑥、⑦、⑨的简单离子的离子半径由大到小的顺序是Cl->Na+>Al3+Cl->Na+>Al3+。(用离子符号填写)
(3)由⑧与⑨形成的某种分子中各原子都满足最外层为8电子结构,其分子式是PCl3PCl3;由⑤与⑨形成的某种化合物中原子最外层均满足8电子结构,用电子式表示该化合物的形成过程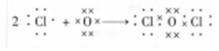
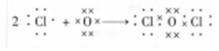 。
。
(4)①、②、⑥的元素符号用X、Y、Z表示,它们所形成的化合物ZYX4的电子式为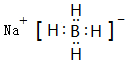
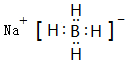 。(用真实的元素符号表示)
。(用真实的元素符号表示)
(5)元素①与④可形成多种化合物,如甲、乙、丙。甲与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸。8.6g甲爆炸分解生成H2和6.72L另一种单质。写出其爆炸的化学方程式:2HN3 撞击 H2+3N22HN3 撞击 H2+3N2;标准状况下乙的密度为0.76g•L-1,乙在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式:2NH3+Fe2O3 高温 N2+2Fe+3H2O2NH3+Fe2O3 高温 N2+2Fe+3H2O;1个丙分子中含有18个电子,丙的结构式为
 。
。
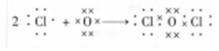
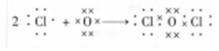
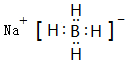
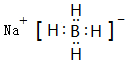
撞击
撞击
高温
高温


【考点】元素周期律和元素周期表的综合应用.
【答案】H2CO3;H3BO3;Cl->Na+>Al3+;PCl3;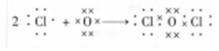 ;
;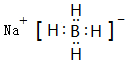 ;2HN3 H2+3N2;2NH3+Fe2O3 N2+2Fe+3H2O;
;2HN3 H2+3N2;2NH3+Fe2O3 N2+2Fe+3H2O;
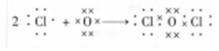 ;
;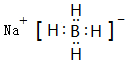 ;2HN3
;2HN3撞击
高温

【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/20 8:0:8组卷:10引用:2难度:0.5
相似题
-
 1.下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
1.下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
(1)元素a和元素b的简单氢化物熔点较高的是a b c d e f (用化学式填空),其原因是.
(2)a和d可形成不同晶体,下列说法正确的是(NA是阿伏加德罗常数).
A.元素a的单质可能是原子晶体或分子晶体
B.mg d元素形成的晶体中,含共价键数目为m NA/7
C.元素a与元素d形成的化合物40g,含NA个分子
D.元素d的最高价氧化物6g,含共价键物质的量为0.4mol
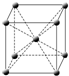
(3)c和e形成的化合物的中,每个阳离子周围距离最近且等距离的阳离子有个,一个晶胞中的阴离子数目为个.晶体中阳离子和阴离子核间距为a cm,该化合物相对分子质量为M,NA为阿伏加德罗常数,则晶体密度为g/cm3.
(4)f原子的外围电子排布式为,其晶胞结构如图,f单质的晶体密度为ρg/cm3,f相对原子质量为M,阿伏加德罗常数NA,则f的原子半径为.发布:2025/1/18 8:0:1组卷:8引用:1难度:0.3 -
2.如图为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
 发布:2024/12/30 18:30:1组卷:8引用:3难度:0.7
发布:2024/12/30 18:30:1组卷:8引用:3难度:0.7 -
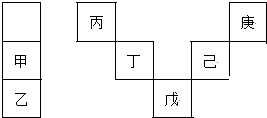
3.甲~庚等元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
 发布:2024/12/30 19:30:2组卷:50引用:5难度:0.7
发布:2024/12/30 19:30:2组卷:50引用:5难度:0.7


