研究人员合成了一种普鲁士蓝(PB)改性的生物炭(BC)复合材料(BC-PB),并将其应用于氨氮废水(含NH3、NH+4)的处理。
资料:
①普鲁士蓝(PB)是亚铁氰化铁的俗称,化学式为Fe4[Fe(CN)6]3,难溶于水。
②BC-PB中,PB负载在BC表面,没有产生新化学键,各自化学性质保持不变。
Ⅰ.复合材料BC-PB的合成

(1)下列关于ⅰ中HCN参与反应的说法正确的是 acac(填字母)。
a.提供H+,与Fe反应
b.提供H+,与OH-反应
c.提供CN-,与Fe2+配位
d.提供CN-,与K+反应
(2)ⅱ中分离得到K4[Fe(CN)6]⋅3H2O的操作包括加热浓缩、冷却结晶、过滤、洗涤、干燥冷却结晶、过滤、洗涤、干燥。
(3)ⅲ中生成普鲁士蓝反应的离子方程式为 3[Fe(CN)6]4-+4Fe3+=Fe4[Fe(CN)6]33[Fe(CN)6]4-+4Fe3+=Fe4[Fe(CN)6]3。
(4)添加造孔剂可以增加BC的孔道数目和容量。造孔剂的造孔原理之一是在一定条件下分解产生气体。700℃时,KHCO3造孔原理的化学方程式为 2KHCO3 △ K2CO3+H2O+CO2↑2KHCO3 △ K2CO3+H2O+CO2↑。
Ⅱ.氨氮废水处理
用NH4Cl溶液模拟氨氮废水。实验发现pH=2时,在BC-PB体系中加入H2O2,可将氨氮转化为无毒气体N2,提高氮氮的去除率。其原理为:
ⅰ.Fe4[Fe(CN)6]3+3H2O2+3H+=3Fe[Fe(CN)6]+Fe3++3⋅OH+3H2O
ⅱ.•OH将氨氮氧化为N2
(5)ⅱ的离子方程式为 6•OH+2NH+4=N2↑+6H2O+2H+6•OH+2NH+4=N2↑+6H2O+2H+。
(6)用BC-PB和H2O混合处理1000L某氨氦含量(以NH4Cl质量计算)为120mg⋅L-1的废水。实验结束后,收集到22.4L N2(已折算成标准状况)。
①实验中消耗的H2O2的质量至少为 204204g。
②处理后的废水中氨氮含量为 1313mg⋅L-1(废水体积变化忽略不计),达到了污水排放标准要求(≤15mg⋅L-1)。
NH
+
4
△
△
2
N
H
+
4
2
N
H
+
4
【答案】ac;冷却结晶、过滤、洗涤、干燥;3[Fe(CN)6]4-+4Fe3+=Fe4[Fe(CN)6]3;2KHCO3 K2CO3+H2O+CO2↑;6•OH+=N2↑+6H2O+2H+;204;13
△
2
N
H
+
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/11 10:0:1组卷:17引用:2难度:0.5
相似题
-
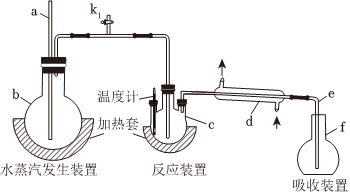 1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5
1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5 -
2.煤气化是有效利用化石能源手段之一,有关反应如下:
①C+H2OCO+H2 ②CO+H2O高温CO2+H2一定条件
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
[实验]使水蒸气通过灼热的焦炭,收集反应后流出的气体。
[提出假设]对气体的成分提出了三种假设。
假设1:该气体是 CO、H2。
假设2:该气体是 CO、H2、H2O。
(1)假设3:。
[设计实验方案,验证假设]
他们拟用下图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)。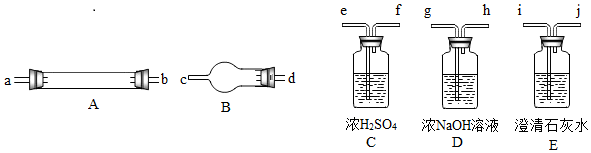
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):
混合气→dc→→→ij→→→→ij;
(3)仪器A中需加入试剂的是,其中反应的化学方程式是;
(4)仪器B中需加入试剂的名称是,其作用是;
[思考与交流]
(5)本实验的尾气需要处理,处理的方法为。
(6)某同学认为增加焦炭的量可以提高化学反应①的速率,你是否同意他的说法,并简述理由。发布:2024/12/30 14:0:1组卷:34引用:4难度:0.5 -
3.为探究矿石样品X(仅含两种元素)的组成和性质,某同学设计并完成如图实验:
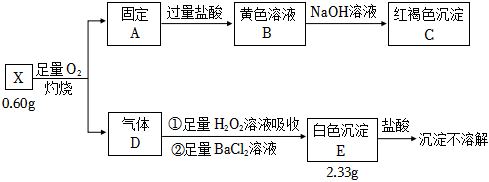
请回答:
(1)X含有的元素。
(2)X的化学式。
(3)红褐色沉淀C是。
(4)气体D通入足量H2O2中发生反应①的化学方程式。发布:2024/12/30 14:30:1组卷:16引用:3难度:0.7


