化学课上老师进行以下实验探究分子的特性。

如图1,烧杯甲中装有20mL蒸馏水,并滴入了几滴酚酞,在烧杯乙中装有10mL浓氨水。用一个大烧杯将甲、乙两个小烧杯罩在一起。一段时间后,甲烧杯中的溶液由无色变为红色。关于酚酞变红,同学们提出了三种猜想:
猜想一:从乙烧杯中蒸发出水蒸气,部分水分子运动进入甲烧杯,水使酚酞变红。
猜想二:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯,氨气使酚酞变红。
猜想三:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯与水结合形成氨水,氨水使酚酞变红。
(1)同学们经过讨论后一致认为猜想一是不可能的,理由是 甲烧杯中本来就有水,开始甲烧杯中的溶液不变红,就说明水不能使酚酞变红甲烧杯中本来就有水,开始甲烧杯中的溶液不变红,就说明水不能使酚酞变红。
(2)为了探究另外两种猜想是否正确,同学们设计了如下实验方案,请补充下表:
| 实验操作 | 实验现象 | 实验结论 | |
| 将一张滤纸浸入酚酞溶液中,1分钟后取出,悬挂在通风处晾干,用剪刀将其剪成两片 | 将其中一片干燥滤纸放入收集满氨气的集气瓶中 | 滤纸不变色 | 猜想 三 三 正确 |
| 在另一片滤纸上滴几滴蒸馏水,再放入收集满氨气的集气瓶中 | 滤纸变成红色 | ||
【进行实验】
改进装置如图2所示(夹持装置已省略)。在U形管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL酚酞溶液插入橡皮塞慢慢注入棉纱布B中,使其润湿;在另一管口插入吸取了2mL浓氨水的注射器并注入棉纱布A中。
【分析讨论】
(3)几分钟后看到的现象是
棉纱布B变红
棉纱布B变红
。(4)通过该实验可得出分子具有的特性是
分子在不断运动
分子在不断运动
。【拓展延伸】
同学们经过讨论后认为,仅通过上述实验并不能得出影响分子运动快慢的因素,于是又设计了两个实验。
实验1:
组装一套与图2装置完全相同的装置(如图3),并用热毛巾捂住插有浓氨水注射器的管口,用图2、图3装置同时进行实验。
(5)实验现象是
棉纱布D和棉纱布B均变红,且棉纱布D比棉纱布B先变红
棉纱布D和棉纱布B均变红,且棉纱布D比棉纱布B先变红
。该现象说明分子运动速率与温度的关系是 相同条件下,温度越高,分子运动速率越快
相同条件下,温度越高,分子运动速率越快
。实验2:
已知氯化氢分子的质量大于氨气分子的质量。如图4将装置平放在桌面上,同时用注射器分别向棉纱布上注入等量的浓氨水和浓盐酸。过一会儿后,观察到产生的白烟并不是在U形管的中间位置,而在如图所示位置。
(6)该现象说明分子运动速率与分子质量的关系是
相同条件下,分子质量越小,分子运动速率越快
相同条件下,分子质量越小,分子运动速率越快
。【答案】甲烧杯中本来就有水,开始甲烧杯中的溶液不变红,就说明水不能使酚酞变红;三;棉纱布B变红;分子在不断运动;棉纱布D和棉纱布B均变红,且棉纱布D比棉纱布B先变红;相同条件下,温度越高,分子运动速率越快;相同条件下,分子质量越小,分子运动速率越快
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/18 8:0:9组卷:31引用:2难度:0.5
相似题
-
1.碳酸氢钠是一种应用广泛的盐,化学小组对其进行了探究。
(1)NaHCO3可称为钠盐或碳酸氢盐,它是由Na+和(填离子符号)构成,医疗上能用于治疗胃酸(含有盐酸)过多症,反应的化学方程式为。
【提出问题】实验室中如何制取少量NaHCO3?
【查阅资料】
材料一:侯氏制碱的原理:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。△
材料二:研究发现,NaHCO3溶于水时吸收热量,Na2CO3溶于水时放出热量。
【实验制备】根据侯氏制碱原理设计如图1所示装置制取NaHCO3。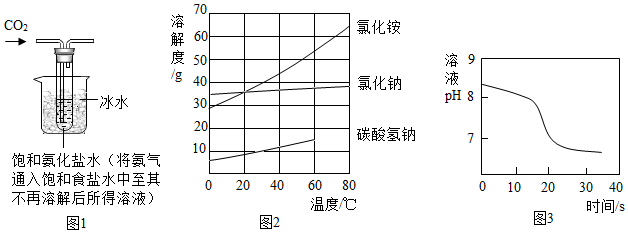
反应结束后,将试管中的混合物过滤洗涤,低温烘干得白色固体。
(2)烧杯中冰水的作用是。
(3)能进一步确认该白色固体是NaHCO3的实验方案是(须用到的仪器和药品:试管、温度计、水)。
(4)如图2中碳酸氢钠的溶解度在60℃后无数据的原因可能是。
【性质探究】
常温下,取一定量的NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图3所示。
【查阅资料】
材料三NaHCO3溶于水后,少量的能同时发生如下变化:HCO-3
变化①:+H2O→H2CO3+OH-;HCO-3
变化②:→HCO-3+H+。CO2-3
材料四:溶液的酸碱性与溶液中H+和OH-数目的相对大小有关。常温下,当单位体积溶液中OH-的数目大于H+的数目时溶液的pH>7,反之pH<7;单位体积溶液中所含的H+数目越大,溶液的pH越小。
【交流反思】
(5)NaHCO3溶液显(填“酸”“碱”或“中”)性,结合材料三、四从微观角度说明原因:。
(6)根据本实验,下列说法错误的是(填字母)。
a.pH<6.68时生成的无色气体为CO2
b.从0~30s,单位体积溶液中H+数目不断增大
c.不能用CaCl2溶液鉴别Na2CO3和NaHCO3溶液发布:2024/12/25 15:30:1组卷:590引用:4难度:0.5 -
2.关于盐的性质研究是一项重要的课题,某兴趣小组以“探究碳酸氢钠的性质”为主题开展项目式学习。
【任务一】认识碳酸氢钠
(1)下列关于碳酸氢钠的说法正确的是。
A.碳酸氢钠是由Na+和构成HCO-3
B.碳酸氢钠俗称纯碱
C.碳酸氢钠医疗上能用于治疗胃酸过多症
D.碳酸氢钠难溶于水
【任务二】探究碳酸氢钠的性质
(2)探究碳酸氢钠与稀盐酸反应:兴趣小组取适量碳酸氢钠粉末于甲试管中,加入稀盐酸,如图1所示,观察到甲试管中有气泡产生,乙中,说明碳酸氢钠能与稀盐酸反应生成CO2,写出试管甲中反应的化学方程式。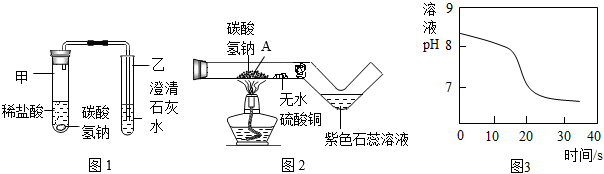
(3)探究碳酸氢钠的热稳定性:用酒精灯充分加热玻璃管,如图2所示。
资料:无水硫酸铜呈白色,遇水后呈蓝色
①发现玻璃管内无水硫酸铜变蓝,紫色石蕊溶液变红,说明碳酸氢钠受热易分解,且有和二氧化碳生成。
②实验后兴趣小组同学猜想玻璃管A处固体产物仅是Na2CO3而不含有NaOH,请设计实验证明(写出具体步骤和现象):。
(4)常温下,兴趣小组同学取一定量的NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图3所示。
【查阅资料】
材料一:NaHCO3溶于水后,少量的能同时发生如下变化:HCO-3
变化①:+H2O→H2CO3+OH-HCO-3
变化②:→HCO-3+H+CO2-3
材料二:溶液的酸碱性与溶液中H+和OH-数目的相对大小有关。常温下,当单位体积溶液中OH-的数目大于H+的数目时溶液的pH>7,反之pH<7;单位体积溶液中所含的H+数目越大,溶液的pH越小。
①根据上述实验可知NaHCO3溶液显碱性,结合材料一、二从微观角度说明原因:。
②根据本实验,可知从0~30s,单位体积溶液中H+数目不断(填“增大”或“减小”)。发布:2024/12/25 17:0:2组卷:94引用:2难度:0.4 -
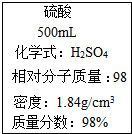 3.图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.
3.图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.
[查阅资料]浓硫酸有强腐蚀性,溶于水会放热;硫酸钡不溶于水也不溶于酸.
[探究一]浓硫酸稀释时会放热.
(1)稀释浓硫酸时,所需仪器主要有,应如何稀释浓硫酸?.测量稀释前后溶液的温度,有明显升高的现象.结论:浓硫酸溶于水放热.
[探究二]稀硫酸与氢氧化钠溶液能发生反应.图10
(2)稀硫酸与氢氧化钠溶液反应的化学方程式为实验步骤 实验现象 实验结论 先用pH试纸测定稀硫酸的pH,再逐滴加入氢氧化钠溶液并不断振荡,同时测混合液的pH pH逐渐变大,
最后pH≥7稀硫酸与氢氧化钠
溶液能发生反应.
(3)实验中仅从溶液pH变大,而不强调pH≥7,不能得出稀硫酸与氢氧化钠溶液一定发生反应的结论,理由是.
[探究三]由于该试剂瓶瓶口密封签已破损,同学们怀疑该浓硫酸的质量分数与标签不相符.
[提出问题]该浓硫酸的质量分数是否发生变化?
[实验探究](4)取该浓硫酸和足量BaCl2溶液反应,过滤、洗涤、干燥沉淀.实验中如何确定硫酸已完全反应.
(5)为达到实验目的,实验中必须要测知的数据是.
[探究结论](6)由实验测得的数据计算出的硫酸的质量分数与标签不符.该硫酸的质量分数应98%(填“大于”或“小于”).发布:2025/1/6 8:0:1组卷:38引用:1难度:0.5


