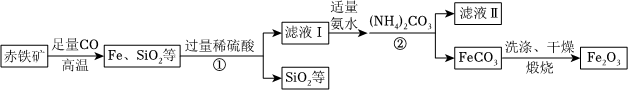
高纯氧化铁(Fe2O3)又称“引火铁”,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程示意图,请回答相关问题。
【资料卡片】:
①氨水呈碱性(主要成分NH3•H2O是一种碱);(NH4)2CO3溶液呈碱性,40℃以上易分解。
②FeCO3高温 FeO+CO2↑,4FeO+O2=2Fe2O3
(1)赤铁矿炼铁的方程式为 3CO+Fe2O3 高温 2Fe+3CO23CO+Fe2O3 高温 2Fe+3CO2。
(2)加适量氨水的目的是 除去过量的稀硫酸除去过量的稀硫酸。
(3)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是 反应温度不超过40℃反应温度不超过40℃。
(4)滤液Ⅱ中可回收的产品是 (NH4)2SO4(NH4)2SO4(写化学式),该物质的用途是 作氮肥(化肥)作氮肥(化肥)。
(5)有同学认为可以向滤液Ⅰ中通入CO2和NH3也能实现同样反应。某学习小组利用如图装置模拟此反应。
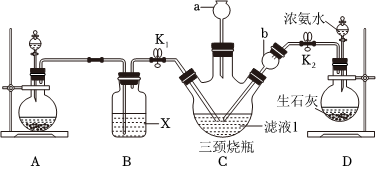
①图A为实验室制备CO2的装置,其药品的最佳选择为 ACAC(填序号)。
A.石灰石
B.CaCO3
C.稀盐酸
D.稀硫酸
②B装置为除去二氧化碳中的氯化氢气体,洗气瓶中的试剂X可选择 BCBC(填序号)。
A.NaOH溶液
B.饱和NaHCO3溶液
C.AgNO3溶液
D.浓硫酸
③C装置中长颈漏斗a的作用是 平衡装置内气压平衡装置内气压,在其上端需要放一团沾有酸液的棉花团其原因是 吸收逸出的氨气,防止污染空气吸收逸出的氨气,防止污染空气,长颈漏斗b的作用是 防倒吸防倒吸。
(6)写出在空气中煅烧FeCO3的化学反应方程式 4FeCO3+O2 高温 2Fe2O3+4CO24FeCO3+O2 高温 2Fe2O3+4CO2。
(7)该流程中使用稀硫酸的质量分数为19.6%,若用含Fe2O380%的赤铁矿1.5t作为原料,则理论上参加反应的稀硫酸的质量是多少?(写出计算过程)
高温
高温
高温
高温
高温
【答案】3CO+Fe2O3 2Fe+3CO2;除去过量的稀硫酸;反应温度不超过40℃;(NH4)2SO4;作氮肥(化肥);AC;BC;平衡装置内气压;吸收逸出的氨气,防止污染空气;防倒吸;4FeCO3+O2 2Fe2O3+4CO2
高温
高温
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/31 8:0:9组卷:43引用:2难度:0.4
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
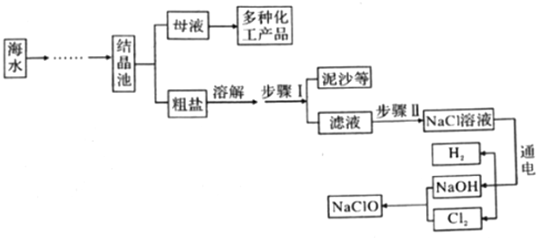
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
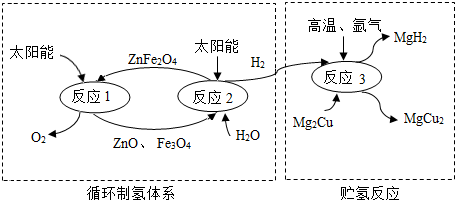 2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5 -
3.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7


