 C1化学又称一碳化学,研究以含有一个碳原子的物质为原料合成工业产品的有机化学及工艺,因其在材料科学和开发清洁燃料方面的重要作用已发展成为一门学科。燃煤废气中的CO、CO2均能转化为基础化工原料、清洁能源甲醇。一定条件下,在恒压密闭容器中投入9molCO和15molH2,催化剂作用下充分反应,CH3OH在平衡混合气中的体积分数在不同压强下随温度的变化如图所示:
C1化学又称一碳化学,研究以含有一个碳原子的物质为原料合成工业产品的有机化学及工艺,因其在材料科学和开发清洁燃料方面的重要作用已发展成为一门学科。燃煤废气中的CO、CO2均能转化为基础化工原料、清洁能源甲醇。一定条件下,在恒压密闭容器中投入9molCO和15molH2,催化剂作用下充分反应,CH3OH在平衡混合气中的体积分数在不同压强下随温度的变化如图所示:
(1)该反应的平衡常数为K═c(CH3OH)[c(CO)c2(H2)]则化学方程式为 CO(g)+2H2(g)⇌CH3OH(g)CO(g)+2H2(g)⇌CH3OH(g),该反应的ΔH <<0,ΔS <<0(填“>”“=”或“<”)。
(2)P1、P2、P3由大到小的顺序为 P1>P2>P3P1>P2>P3,计算A点的压强平衡常数Kp═350P22350P22(用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(3)300℃,P2条件下,处于E点时反应的方向是 正反应正反应(填“正反应”“逆反应”或“平衡状态”)。
(4)某温度下,能说明该反应已经达到平衡状态的是 DEDE(填序号)。
A.容器内各组分浓度相等
B.速率之比v(CO):v(H2):v(CH3OH)=1:2:1
C.H2的消耗速率等于CH3OH的消耗速率
D.容器内混合气体的平均相对分子质量不再变化
E.容器内的密度不再变化
c
(
C
H
3
OH
)
[
c
(
CO
)
c
2
(
H
2
)
]
350
P
2
2
350
P
2
2
【答案】CO(g)+2H2(g)⇌CH3OH(g);<;<;P1>P2>P3;;正反应;DE
350
P
2
2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/17 8:0:8组卷:12引用:2难度:0.5
相似题
-
1.反应 4A(g)+5B(g)⇌4C(g)+6D(g)在 5L 的密闭容器中进行,半分钟后,C 的物质的量增 加了 0.30mol。下列叙述正确的是( )
发布:2024/12/30 19:30:2组卷:67引用:6难度:0.6 -
2.氢气最早于16世纪被人工制取出来,氢气是一种清洁能源。
(1)利用光伏电池电解水制H2是氢能的重要来源。已知:H-H键、O=O键、H-O键的键能依次为436kJ•mol-1、495kJ•mol-1、463kJ•mol-1。则2H2O(g)═2H2(g)+O2(g)△H=kJ•mol-1。
(2)T1℃时,向5L恒容密闭容器中充入0.5molCH4,只发生反应2CH4(g)⇌C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=2c(CH4),CH4的转化率为;保持其他条件不变,温度改为T2℃,经25s后达到平衡,测得c(CH4)=2c(C2H4),则0~25s内v(C2H4)=mol•L-1•s-1。
(3)CH4分解时几种气体的平衡分压(pPa)的对数值lgp与温度的关系如图所示。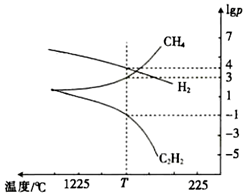
①T℃时,向一恒容密闭容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只发生反应2CH4(g)⇌C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此时的平衡常数Kp=(用平衡分压代替浓度进行计算)Pa2。
②若只改变一个反应条件使Kp变大,则该条件是(填标号)。
A.减小C2H2的浓度
B.升高温度
C.增大压强
D.加入合适的催化剂
(4)工业上,以KNH2和液氨为电解质,以石墨为电极,电解液氨制备H2。阳极的电极反应式为,一段时间后阴、阳两极收集到的气体质量之比为。发布:2025/1/4 8:0:1组卷:9引用:3难度:0.5 -
3.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(L•min);
(3)x的值为.发布:2024/12/30 19:0:1组卷:163引用:26难度:0.3


