随着常规能源的有限性以及环境问题的日益突出,以环保和可再生为特质的新能源越来越得到各国的重视。新能源的使用与研究在一定程度上助力中国实现“碳达峰、碳中和”。
(1)铅酸电池,其结构如图所示,放电时的电池反应:PbO2+Pb+2H2SO4=2PbSO4+2H2O.根据此反应判断下列叙述中正确的是 BB。
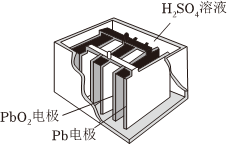
A.PbO2是电池的负极
B.Pb是负极
C.PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
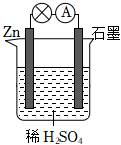
(2)由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的pH值 DD。
A.不变
B.先变小后变大
C.逐渐变小
D.逐渐变大
(3)港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是 CC。
A.防腐原理主要是避免发生反应:2Fe+O2+2H2O=2Fe(OH)2
B.钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等防止形成原电池
C.采用外加电流的阴极保护时需外接镁、锌等活泼金属做阳极
D.钢构件可采用不锈钢材料以减缓电化学腐蚀
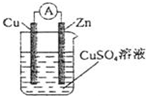
(4)用如图装置可以模拟铁的电化学防护,下列说法不正确的是 AA。
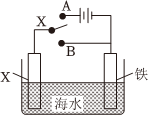
A.若X为锌棒,开关K置于B处时,铁电极反应为2H++2e-=H2↑
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为碳棒,开关K置于A处时,铁电极反应2H2O+2e-=H2↑+2OH-
D.若X为碳棒,开关K置于A处可以减缓铁的腐蚀
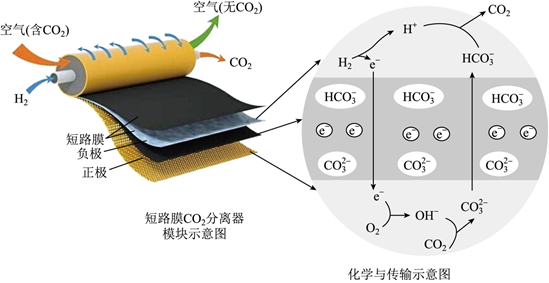
(5)如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少,请回答:
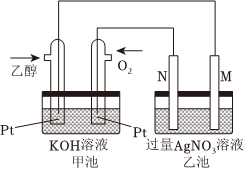
①甲池中通入乙醇的铂电极名称是 负极负极,通入O2的铂电极反应式为 O2+2H2O+4e-=4OH-O2+2H2O+4e-=4OH-;
②乙池属于 电解池电解池(填“原电池”或“电解池”),工作时,乙池中电子流出的电极是 NN(填“M”或“N”);
③若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为 0.2240.224L(标准状况下);
④如要用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是 粗铜粗铜,反应一段时间以后,CuSO4溶液的浓度 减小减小。(填“增大”“减小”“不变”)
【考点】原电池与电解池的综合;金属的腐蚀与防护.
【答案】B;D;C;A;负极;O2+2H2O+4e-=4OH-;电解池;N;0.224;粗铜;减小
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/24 8:0:9组卷:96引用:1难度:0.6