 化学反应的本质是化学键的断裂和形成。化学反应通常伴随着热效应。
化学反应的本质是化学键的断裂和形成。化学反应通常伴随着热效应。
(1)(单选)下列关于燃料充分燃烧的说法中,错误的是 AA。
A.空气量越多,燃烧效果越好
B.应通入充足且适量的空气
C.固体燃料燃烧前要粉碎
D.液体燃料燃烧时可以以雾状喷出
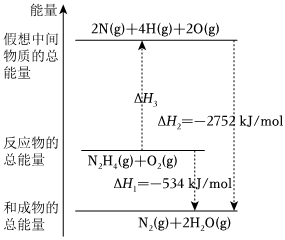
(2)(单选)肼(H2NNH2,各原子间均以单键相连)是一种高能燃料,有关化学反应的能量变化如图所示。已知键能:O=O500kJ⋅mol-1,N-N154kJ⋅mol-1,则N-H键的键能为 BB。
A.194kJ⋅mol-1
B.391kJ⋅mol-1
C.516kJ⋅mol-1
D.658kJ⋅mol-1
(3)(不定项选择)已知反应:
①2C(s)+O2(g)=2CO(g)ΔH=-221kJ⋅mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ⋅mol-1
③H2(g)+12O2(g)=H2O(g)ΔH=-241.8kJ⋅mol-1
④H2O(g)=H2O(l)ΔH=-44.0kJ⋅mol-1
下列结论正确的是 ADAD。
A.碳的燃烧热大于110.5kJ⋅mol
B.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
C.氢气的燃烧热为241.8kJ⋅mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ⋅mol-1
(4)白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
①已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)═P4O10(s)ΔH1=-2983.2kJ⋅mol-1
P(s,红磷)+54O2(g)═14P4O10(s)ΔH2=-738.5kJ⋅mol-1
则该温度下白磷转化为红磷的热化学方程式为 P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/molP4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol。
②已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)═P4O6(s)ΔH=-1638kJ⋅mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为 3:13:1,反应过程中放出的热量为 1323.45kJ1323.45kJ。
(5)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)ΔH1=+64.39kJ⋅mol-1
②2H2O2(l)═2H2O(l)+O2(g)ΔH2=-196.46kJ⋅mol-1
③H2(g)+12O2(g)═H2O(l)ΔH3=-285.84kJ⋅mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 Cu(s)+H2O2(aq)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68kJ/molCu(s)+H2O2(aq)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol。
1
2
5
4
1
4
1
2
【答案】A;B;AD;P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol;3:1;1323.45kJ;Cu(s)+H2O2(aq)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/5 8:0:8组卷:61引用:1难度:0.6
相似题
-
1.氢在地球上主要以化合态的形式存在,是宇宙中分布最广泛的物质,它构成了宇宙质量的75%,属于二次能源.工业上生产氢的方式很多,常见的有水电解制氢,煤炭气化制氢,重油及天然气水蒸气催化制氢等.氢气是一种理想的绿色能源,如图1为氢能产生和利用的途径:
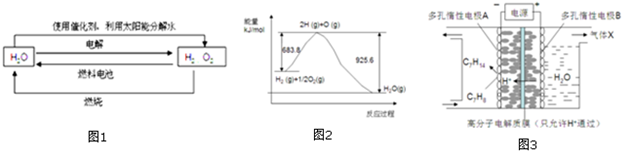
(1)图1的四个过程中能量转化形式有
A.2种 B.3种 C.4种 D.4种以上
(2)电解过程要消耗大量的电能,而使用微生物作催化剂在阳光下也能分解水.
2H2O(1)2H2(g)+O2(g)△H 1 2H2O(1)通电2H2(g)+O2(g)△H2光照催化剂
以上反应的△H1△H2(选填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依据图2能量变化写出氢气燃烧生产液态水的热化学方程式
(4)氢能利用需要选择合适的储氢材料.
①NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
②镧镍合金在一定条件下可吸收氢气生产氢化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)释放出气态氢,根据平衡移动的原理,可改变的条件之一是
③一定条件下,如图3所示装置可实现有机物的电化学储氢,使C7H8转化为C7H14,则电解过程中产生的气体X 为,电极A上发生的电极反应式为.发布:2024/12/17 8:0:2组卷:38引用:1难度:0.5 -
2.肼(N2H4)可作为发射火箭的燃料。已知1g液态肼(N2H4)气体在空气中燃烧生成氮气和水蒸气,放出16.7kJ的热量,该反应的热化学方程式是( )
发布:2024/12/30 3:0:4组卷:121引用:9难度:0.6 -
3.在298K、1.01×105Pa下,将0.5mol CO2通入750mL 1mol•L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知在该条件下,1mol CO2通入1L 2mol•L-1NaOH溶液中充分反应放出ykJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
发布:2024/12/30 4:0:1组卷:143引用:5难度:0.7


