日常生活中我们见到的物质大部分都属于混合物,在化学实验中,我们可以运用物理或化学方法,将混合物中的组分分开再进行提纯从而得到纯净物进一步研究其组成、结构与性质。
(1)下列离子检验方法不合理的是 DD。
A.H+→显色法
B.SO2-4→沉淀法
C.CO2-3→气体法
D.K+→沉淀法
(2)下列物质不能做为碘水萃取剂的是 DD。
A.苯
B.汽油
C.四氯化碳
D.酒精
(3)以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是 CC。

(4)关于仪器使用,说法错误的是 DD。
A.过滤操作应使用玻璃棒引流
B.加热锥形瓶时应垫石棉网
C.振荡分液漏斗时应关闭玻璃塞和活塞
D.蒸馏时温度计水银球的上沿应高于蒸馏烧瓶支管口的下沿
(5)下列有关实验说法不正确的是 BB。
A.用乙醇提取中药里的有效成分属于萃取操作
B.利用蒸发结晶的方法除去KNO3固体中少量的KCl
C.实验室中,可用蒸馏操作除去自来水中少量的Na+、Cl-、SO2-4
D.分液漏斗静置分液时,需打开上口的玻璃塞
(6)能一次性鉴别AgNO3、Na2CO3、NaCl三种溶液的试剂是 AA。
A.盐酸
B.NaOH溶液
C.BaCl2溶液
D.KNO3溶液
(7)下列各组溶液,不用其他试剂就能鉴别的是 ACAC。
A.CuSO4、Na2SO4、BaCl2
B.CuSO4、Ba(NO3)2、BaCl2
C.HCl、Na2CO3、NaOH
D.Na2SO4、BaCl2、Na2CO3
(8)氢氧化钠溶液放置在空气中会部分变质,以下验证其中含有碳酸钠的方法中,错误的是 CC。
A.取样,加入澄清石灰水,有沉淀生成,则含碳酸钠
B.取样,加入少量氯化钡溶液,有白色沉淀生成,则含碳酸钠
C.取样,加入少量盐酸,无气泡产生,则不含碳酸钠
D.取样,加入少量氯化钙溶液,有白色沉淀,则含碳酸钠
(9)下列关于硫酸根离子的检验方法中,正确的是 DD。
A.加入BaCl2溶液,产生白色沉淀,则原溶液中存在SO2-4离子
B.先加BaCl2溶液,再加HCl,产生白色沉淀,则原溶液中存在SO2-4离子
C.加入用HNO3酸化的BaCl2溶液,产生白色沉淀,则原溶液中存在SO2-4离子
D.加入过量HCl酸化,再向澄清液中加入BaCl2溶液,产生白色沉淀,则说明原溶液中存在SO2-4离子
(10)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图:

①在第②③④步中所加试剂均过量,原因是 使杂质沉淀完全使杂质沉淀完全。
②第②步操作加入过量的BaCl2目的是除去粗盐中的 Na2SO4Na2SO4;写出这个反应的化学方程 Na2SO4+BaCl2=BaSO4↓+2NaClNa2SO4+BaCl2=BaSO4↓+2NaCl。
③第⑤步“过滤”操作中得到沉淀的成分有泥沙、BaSO4、BaCO3、CaCO3、Mg(OH)2BaSO4、BaCO3、CaCO3、Mg(OH)2(填化学式)
④在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是 会引入新的杂质会引入新的杂质。
⑤在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去滤液中的NaOH和 Na2CO3Na2CO3。
SO
2
-
4
CO
2
-
3
SO
2
-
4
SO
2
-
4
SO
2
-
4
SO
2
-
4
SO
2
-
4
【答案】D;D;C;D;B;A;AC;C;D;使杂质沉淀完全;Na2SO4;Na2SO4+BaCl2=BaSO4↓+2NaCl;BaSO4、BaCO3、CaCO3、Mg(OH)2;会引入新的杂质;Na2CO3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/6 10:0:2组卷:40引用:1难度:0.6
相似题
-
1.某无色溶液,其中可能存在Na+、Ba2+、
、S2-、AlO-2、SO2-3.取该溶液进行有关实验,实验结果如图所示.SO2-4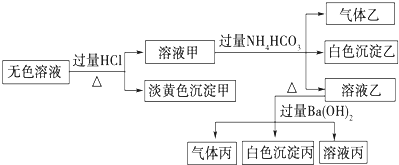
回答下列问题:
(1)沉淀甲的化学式为.
(2)由溶液甲生成沉淀乙的离子方程式为.
(3)沉淀丙中一定含有(填化学式,下同),可能含有.
(4)综合上述信息,该溶液中肯定存在的离子有.
(5)该溶液显性(填酸性、碱性或中性),若要检验其酸碱性,下图操作正确的是.
请用离子方程式表示显碱性的原因:.发布:2024/12/30 6:0:2组卷:10引用:2难度:0.3 -
2.在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化。(填序号)
(1)鉴定氯酸钾中氯元素的操作步骤依次是
(2)鉴定1-氯丙烷中氯元素的操作步骤依次是。发布:2024/12/30 8:0:15组卷:67引用:8难度:0.5 -
3.为检验某种阳离子为Na-的溶液中含有的阴离子是SO42-、CO32-、OH-还是Cl-,下列设计的方案合理的是( )
发布:2024/12/30 6:30:2组卷:9引用:2难度:0.6


