 (1)已知:25℃时,Ksp[Mg(OH)2]=4×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
(1)已知:25℃时,Ksp[Mg(OH)2]=4×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
| PH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
蓝色
蓝色
.②25℃时,向该Mg(OH)2饱和溶液中加入适量稀盐酸达平衡后该溶液中c(OH-)
减小
减小
,c(Mg2+)增大
增大
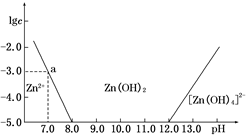
(填“增大”“减小”或“不变”).(2)如图,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-物质的量浓度的对数,回答下列问题.
①往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为
Zn2++4OH-═+2H2O
Z
n
O
2
-
2
Zn2++4OH-═+2H2O
.Z
n
O
2
-
2
②从图中数据计算可得Zn(OH)2的溶度积Ksp=
10-17
10-17
.③某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是
8.0~12.0
8.0~12.0
.(4)莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度.已知:
| 银盐 性质 |
AgCl | AgBr | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 砖红 |
滴入最后一滴标准液时,生成砖红色沉淀,且30s内不褪色
滴入最后一滴标准液时,生成砖红色沉淀,且30s内不褪色
.终点现象对应的离子反应方程式为2Ag++=Ag2CrO4↓
C
r
O
2
-
4
2Ag++=Ag2CrO4↓
.C
r
O
2
-
4
【考点】沉淀溶解平衡.
【答案】蓝色;减小;增大;Zn2++4OH-═+2H2O;10-17;8.0~12.0;滴入最后一滴标准液时,生成砖红色沉淀,且30s内不褪色;2Ag++=Ag2CrO4↓
Z
n
O
2
-
2
C
r
O
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/13 9:0:8组卷:59引用:3难度:0.3
相似题
-
1.已知常温下:KsP(AgCl白色)=1.8×10-10,KsP(Ag2S黑色)=2.0×10-48 KsP(Ag2CrO4红色)=1.9×10-12,下列叙述正确的是( )
发布:2024/12/30 8:0:1组卷:10引用:0难度:0.9 -
2.铁器表面氧化层的成分有多种:致密的Fe3O4、疏松的FeO(OH)和FeOCl,它们均难溶于水.下列说法错误的是( )
发布:2024/12/19 13:30:1组卷:62引用:3难度:0.5 -
3.高中化学《化学反应原理》模块从不同的视角对化学反应进行了探究、分析,以下观点中不正确的是( )
发布:2024/12/30 10:30:1组卷:10引用:4难度:0.7


