当今研发二氧化碳利用技术降低空气中二氧化碳含量成了研究热点。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体CO2,总反应可表示为:
CO2(g)+3H2(g)⇌H2O(g)+CH3OH(g)ΔH
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH1=41kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g)ΔH2=-90kJ/mol
(1)ΔH=-49-49kJ/mol。
(2)一定条件下,向体积为1L的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,反应①的平衡常数为 (a+b)•b(1-a-b)•(3-3a-b)(a+b)•b(1-a-b)•(3-3a-b)(用含a,b的代数式表示)。
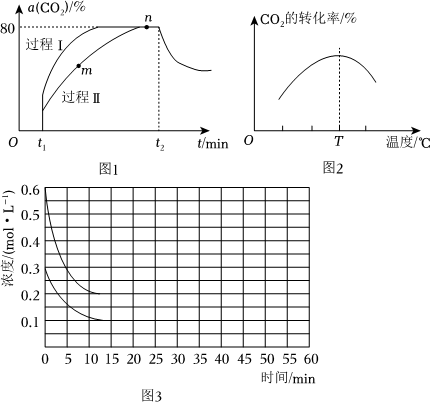
(3)总反应CO2(g)+3H2(g)⇌H2O(g)+CH3OH(g)在Ⅰ、Ⅱ两种不同催化剂作用下建立平衡过程中,CO2的转化率[a(CO2)]随时间(t)的变化曲线如图1。活化能:过程Ⅰ<<过程Ⅱ(填“<”,“>”,),t2时刻改变了某一反应条件,下列说法正确的是 ACAC。
A.恒温恒压,t2时刻通入惰性气体
B.恒温恒容,t2时刻通入一定量氢气
C.n点的v(正)一定大于m点的v(逆)
D.t2时刻,可能是移走了一部分水蒸气
Ⅱ.(4)以CO2和NH3为原料合成尿素[CO(NH2)2]是固定和利用CO2的成功范例。在尿素合成塔中的主要反应(均自发进行)可表示:
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2CO2NH4(s)ΔH1
反应Ⅱ:NH2CO2NH4(s)⇌CO(NH2)2(s)+H2O(g)ΔH2
反应Ⅲ:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g)ΔH3
某研究小组为探究反应Ⅲ影响CO2转化率的因素,在其它条件一定时,图2为CO2转化率受温度变化影响的曲线。当温度高于T℃后,CO2转化率变化趋势如图所示,其原因是 温度高于T℃时,反应达到平衡状态,因为反应Ⅲ为自发反应,而△S<0,则反应ΔH3<0,即该反应为放热反应,温度升高,平衡逆向移动,CO2的平衡转化率降低温度高于T℃时,反应达到平衡状态,因为反应Ⅲ为自发反应,而△S<0,则反应ΔH3<0,即该反应为放热反应,温度升高,平衡逆向移动,CO2的平衡转化率降低。(不考虑催化剂活性变化)
(5)在某恒定温度下,将NH3和CO2物质的量之比按2:1充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计且只发生反应Ⅰ),经15min达到平衡,各物质浓度的变化曲线图3所示。若保持平衡的温度和体积不变,25min时再向该容器中充入2molNH3和1molCO2,在40min时重新达到平衡,请在如图3中画出25-50min内CO2的浓度变化趋势曲线。 
 。
。
(
a
+
b
)
•
b
(
1
-
a
-
b
)
•
(
3
-
3
a
-
b
)
(
a
+
b
)
•
b
(
1
-
a
-
b
)
•
(
3
-
3
a
-
b
)


【答案】-49;;<;AC;温度高于T℃时,反应达到平衡状态,因为反应Ⅲ为自发反应,而△S<0,则反应ΔH3<0,即该反应为放热反应,温度升高,平衡逆向移动,CO2的平衡转化率降低;
(
a
+
b
)
•
b
(
1
-
a
-
b
)
•
(
3
-
3
a
-
b
)

【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/5 5:0:2组卷:20引用:1难度:0.4
相似题
-
1.反应 4A(g)+5B(g)⇌4C(g)+6D(g)在 5L 的密闭容器中进行,半分钟后,C 的物质的量增 加了 0.30mol。下列叙述正确的是( )
发布:2024/12/30 19:30:2组卷:67引用:6难度:0.6 -
2.氢气最早于16世纪被人工制取出来,氢气是一种清洁能源。
(1)利用光伏电池电解水制H2是氢能的重要来源。已知:H-H键、O=O键、H-O键的键能依次为436kJ•mol-1、495kJ•mol-1、463kJ•mol-1。则2H2O(g)═2H2(g)+O2(g)△H=kJ•mol-1。
(2)T1℃时,向5L恒容密闭容器中充入0.5molCH4,只发生反应2CH4(g)⇌C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=2c(CH4),CH4的转化率为;保持其他条件不变,温度改为T2℃,经25s后达到平衡,测得c(CH4)=2c(C2H4),则0~25s内v(C2H4)=mol•L-1•s-1。
(3)CH4分解时几种气体的平衡分压(pPa)的对数值lgp与温度的关系如图所示。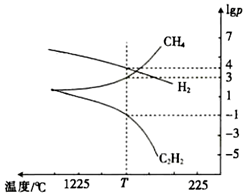
①T℃时,向一恒容密闭容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只发生反应2CH4(g)⇌C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此时的平衡常数Kp=(用平衡分压代替浓度进行计算)Pa2。
②若只改变一个反应条件使Kp变大,则该条件是(填标号)。
A.减小C2H2的浓度
B.升高温度
C.增大压强
D.加入合适的催化剂
(4)工业上,以KNH2和液氨为电解质,以石墨为电极,电解液氨制备H2。阳极的电极反应式为,一段时间后阴、阳两极收集到的气体质量之比为。发布:2025/1/4 8:0:1组卷:9引用:3难度:0.5 -
3.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(L•min);
(3)x的值为.发布:2024/12/30 19:0:1组卷:163引用:26难度:0.3


