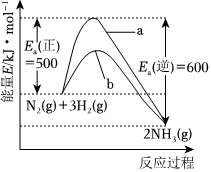
 如图表示298.15K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:
如图表示298.15K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:
(1)若反应中生成2mol氨,则反应 放热放热(填“吸热”或“放热”) 9292kJ。
(2)图中曲线 bb(填“a”或“b”)表示加入铁触媒(催化剂)的能量变化曲线,铁触媒能加快反应速率的原理是 改变反应历程,降低了合成氨反应的活化能改变反应历程,降低了合成氨反应的活化能。
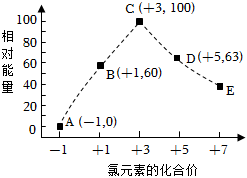
(3)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如图所示。若曲线a对应的温度为500℃,则曲线b对应的温度可能是 DD(填字母)。
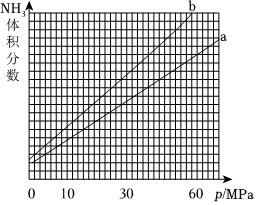
A.600℃
B.550℃
C.500℃
D.450℃
(4)合成氨所需的氢气可由甲烷与水反应制备.发生反应为CH4(g)+H2O(g)⇌CO(g)+3H2(g)ΔH>0。一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
| t/min | CH4/mol⋅L-1 | H2O/mol⋅L-1 | CO/mol⋅L-1 | H2/mol⋅L-1 |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.3 |
| 3 | n1 | n2 | n3 | 0.3 |
| 4 | 0.09 | 0.19 | x | 0.33 |
0.11
0.11
mol⋅L-1;前2min内H2O的平均反应速率为 0.05mol⋅L-1⋅min-1
0.05mol⋅L-1⋅min-1
。②反应在3~4min之间,氢气的物质的量增多的原因可能是
C
C
(填字母)。A.充入水蒸气
B.缩小体积增大压强
C.升高温度
D.充入氢气
【答案】放热;92;b;改变反应历程,降低了合成氨反应的活化能;D;0.11;0.05mol⋅L-1⋅min-1;C
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/2 3:0:2组卷:27引用:2难度:0.5