将足量SO2通入AgNO3溶液中,产生沉淀。探究反应原理及沉淀成分,装置如图(加热,夹持等装置略)。
资料:i.Ag2SO4微溶于水;Ag2SO3难溶于水。
ii.Ag2SO4、Ag2SO3均溶于氨水。

(1)①A中反应的化学方程式是 Cu+2H2SO4(浓) △ CuSO4+SO2↑+2H2OCu+2H2SO4(浓) △ CuSO4+SO2↑+2H2O。
②用NaOH溶液吸收尾气中的SO2产物是 Na2SO3Na2SO3。
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
C
u
+
2
H
2
S
O
4
(
浓
)
△
C
u
S
O
4
+
S
O
2
↑
+
2
H
2
O
C
u
+
2
H
2
S
O
4
(
浓
)
△
C
u
S
O
4
+
S
O
2
↑
+
2
H
2
O
| 时间 | 反应开始时(t1) | 一段时间后(t2) | 较长时间后(t3) |
| 颜色 | 白色 | 灰黑色 | 灰黑色加深 |

实验证实,白色沉淀(t1)中不含Ag2SO4,含Ag2SO3。
①试剂a是
BaCl2溶液
BaCl2溶液
。②产生白色沉淀Y的原因是
酸性条件下,有氧化性
N
O
-
3
酸性条件下,有氧化性
。N
O
-
3
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤,洗涤。向洗净的沉淀中加入浓HNO3,证实沉淀含Ag。现象是
沉淀溶解,产生红棕色气体
沉淀溶解,产生红棕色气体
。(4)通过检测
S
O
2
-
4
①实验:
 (已排除O2的影响)
(已排除O2的影响)t2时,C中H2SO3的作用是
H2SO3+Ag2SO3═2Ag↓+H2SO4+SO2↑
H2SO3+Ag2SO3═2Ag↓+H2SO4+SO2↑
。(用化学方程式表示)②t1时,C中产生白色沉淀的离子方程式是
S
O
2
+
H
2
O
+
2
A
g
+
═
A
g
2
S
O
3
↓
+
2
H
+
S
O
2
+
H
2
O
+
2
A
g
+
═
A
g
2
S
O
3
↓
+
2
H
+
(5)综上可知,化学反应的产物与反应速率和限度有关。
【考点】性质实验方案的设计.
【答案】 ;Na2SO3;BaCl2溶液;酸性条件下,有氧化性;沉淀溶解,产生红棕色气体;H2SO3+Ag2SO3═2Ag↓+H2SO4+SO2↑;
C
u
+
2
H
2
S
O
4
(
浓
)
△
C
u
S
O
4
+
S
O
2
↑
+
2
H
2
O
N
O
-
3
S
O
2
+
H
2
O
+
2
A
g
+
═
A
g
2
S
O
3
↓
+
2
H
+
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/26 8:0:9组卷:75引用:2难度:0.5
相似题
-
1.如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
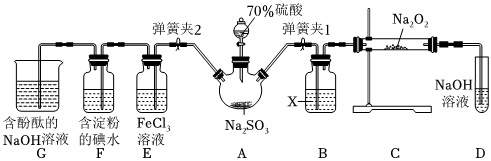
(1)在组装好装置后,若要检验A~D装置的气密性,其操作是首先,然后往D中装入水,然后微热A,观察到D中有气泡冒出,移开酒精灯或松开双手,D中导管有水柱形成且高度保持不变,说明装置气密性良好。
(2)装置D中盛放NaOH溶液的作用是。
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为;发生反应的离子方程式是。
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应。上述方案是否合理?(填“合理”或“不合理”),原因是。
(5)实验过程中G中含酚酞的NaOH溶液逐渐褪色,此实验证明SO2具有漂白性还是其溶于水显酸性?请设计实验验证:。发布:2024/12/30 14:0:1组卷:29引用:2难度:0.5 -
2.某化学兴趣小组为探究铜跟浓硫酸的反应,用图装置进行有关实验.请回答下列问题:
(1)装置A中发生的化学反应的化学方程式为.
(2)装置B 的作用是贮存多余的气体,B中广口瓶内应盛放的液体是(填序号)
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和的NaHSO3溶液
(3)装置C和D 中产生的现象相同,但原因却不同.用离子方程式和必要的文字解释C中溶液褪色的原因
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,这种液体是.
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色.为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中对实验目的没有意义的是(填序号)
①观察稀H2SO4 溶液呈无色 ②观察CuSO4 粉末呈白色 ③稀释CuSO4溶液,溶液蓝色变浅 ④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色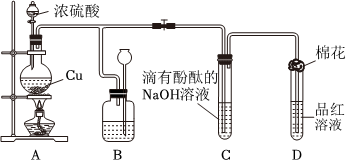 发布:2024/12/30 14:30:1组卷:13引用:2难度:0.7
发布:2024/12/30 14:30:1组卷:13引用:2难度:0.7 -
 3.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
3.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:与盐酸反应最剧烈,与盐酸反应产生的气体最多。(填元素符号)
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为:。
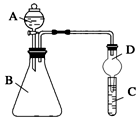
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律
(1)仪器A的名称为。
(2)实验室中现有药品:①稀盐酸 ②稀硝酸 ③Na2SiO3溶液 ④Na2CO3固体,请选择合适药品设计实验验证 N、C、Si的非金属性的变化规律;装置A、B中所装药品分别为、。(填序号)但有同学认为该装置有缺陷,如何改进?。发布:2024/12/30 14:30:1组卷:19引用:2难度:0.5


