元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。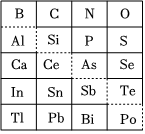
Ⅰ.如图是元素周期表的一部分,回答下列问题。
(1)硒在元素周期表中的位置是:第 四四周期第 ⅥAⅥA族;
(2)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。SeS2中硫元素的化合价为负价,请从原子结构角度解释原因:S元素的非金属性大于Se,得电子能力强S元素的非金属性大于Se,得电子能力强。
(3)可在图中分界线(虚线)附近寻找 BB(填序号)。
A.优良的催化剂
B.半导体材料
C.合金材料
Ⅱ.随着原子序数的递增,七种短周期元素的原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。请回答下列问题:
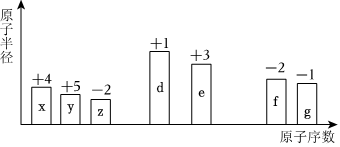
(4)x的氢化物中含有的化学键类型为 共价键共价键(填“离子键”或“共价键”)。
(5)z、d、e的简单离子半径由大到小的顺序为 O2->Na+>Al3+O2->Na+>Al3+(用离子符号表示)。
(6)d的单质在空气中充分燃烧,所得产物的化学式为 Na2O2Na2O2。
(7)e的单质化学性质活泼,但在空气中能稳定存在,也能用于制作炊具的原因是 铝表面形成致密氧化膜,阻止铝继续氧化铝表面形成致密氧化膜,阻止铝继续氧化。(可用化学方程式表示,也可用文字说明)
(8)能说明g的非金属性比f的强的实验事实是 HClO4的酸性比H2SO4强等HClO4的酸性比H2SO4强等(列举一条)。
【答案】四;ⅥA;S元素的非金属性大于Se,得电子能力强;B;共价键;O2->Na+>Al3+;Na2O2;铝表面形成致密氧化膜,阻止铝继续氧化;HClO4的酸性比H2SO4强等
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/22 8:0:8组卷:62引用:1难度:0.7


