铁元素存在于岩石与生命体中,不同价态的铁元素在生产、生活乃至生命活动中有独特的作用。
(1)下列反应能得到单质铁的是 BCBC。
A.Cu与FeCl3溶液反应
B.在高温下Al与Fe3O4反应
C.在高温下CO与Fe2O3反应
D.Fe(OH)3受热分解
(2)能说明Fe的还原性弱于Na的是 CC。
A.Na的熔点比Fe的熔点低
B.1mol的Fe、Na分别与S反应,Fe失电子数多
C.Na与冷水剧烈反应,Fe与冷水不反应
D.Fe3+氧化性强于Na+
(3)实验室盛放FeSO4溶液的试剂瓶中通常需要加入少量铁粉,铁粉的作用是 和铁离子反应生成亚铁离子,防止亚铁离子被氧化和铁离子反应生成亚铁离子,防止亚铁离子被氧化。
水处理厂可用Fe2(SO4)3制备的Na2FeO4对水进行杀菌、消毒等。
(4)Fe2(SO4)3制备Na2FeO4时,从氧化还原角度考虑,不可能用到的物质是 CDCD。
A.NaClO
B.Na2O2
C.Na2S
D.Na2SO3
Fe2(SO4)3溶液也可用于处理工业尾气SO2。将SO2缓慢通入Fe2(SO4)3溶液至过量,观察到溶液由黄色变红棕色,静置后变为浅绿色。由资料知Fe2(SO4)3和SO2发生如下反应:
①Fe3++6SO2⇌[Fe(SO2)6]3+(红棕色)
②22Fe3++11SO2+1H2O1H2O=22Fe2+(浅绿色)+11SO2-4+22H+
(5)请补全、配平反应②,并标出电子转移的数目和方向 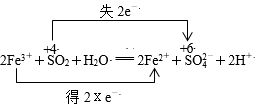
 。
。
(6)实验中,溶液由黄色变为红棕色的过程中也可能有Fe(OH)3胶体生成,请写出检验是否有胶体生成的方法 取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路。
(7)浅绿色溶液中可能混有SO2,请写出检验该溶液中混有SO2的方法 取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2。
(8)请从化学反应速率与化学平衡移动的角度解释向Fe2(SO4)3溶液中通入SO2的实验现象 通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色。
SO
2
-
4


【答案】BC;C;和铁离子反应生成亚铁离子,防止亚铁离子被氧化;CD;2;1;1H2O;2;1;2; ;取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路;取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2;通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色
;取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路;取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2;通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色
 ;取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路;取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2;通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色
;取少量样品于试管中,用激光笔照射样品,看是否有一条光亮的通路;取少量绿色溶液加入品红溶液中,看是否褪色,若褪色,说明含有SO2;通入SO2的过程相当于增加了反应物的浓度,正反应速率大于逆反应速率,平衡向正反应方向移动,静置相当于给体系减小压强,平衡向逆反应方向移动,产生的SO2和Fe3+发生反应②,生成Fe2+,溶液变为浅绿色【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/23 8:0:10组卷:76引用:1难度:0.5
相似题
-
1.草酸又称乙二酸,化学式为H2C2O4,菠菜中广泛存在,有很强的还原性,能被氧化剂氧化成CO2,如:可以使KMnO褪色,反应过程如下,请先配平,再标出电子转移的数目和方向.
H2C2O4++MnO-4H+-Mn2++CO2↑+H2O.发布:2024/11/29 8:0:2组卷:21引用:1难度:0.5 -
 2.磷单质及其化合物的有广泛应用.
2.磷单质及其化合物的有广泛应用.
(1)三聚磷酸可视为三个磷酸分子(磷酸结构式见图)之间脱去两个分子产物,其结构式为.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为
(2)次磷酸钠(NaH2PO2)可用于化学镀镍.
①NaH2PO2中P元素的化合价为.
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)Ni2++H2PO2-+→Ni++H2PO3-+
(b)6H2PO2-+2H+=2P+4H2PO3-+3H2↑发布:2024/11/19 8:0:1组卷:44引用:1难度:0.5 -
 3.磷单质及其化合物有广泛应用.
3.磷单质及其化合物有广泛应用.
(1)三聚磷酸可视为三个磷酸分子(磷酸结构式见图)之间脱去两个水分子产物,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为.
(2)次磷酸钠(NaH2PO2)可用于化学镀镍.
①NaH2PO2中P元素的化合价为.
②化学镀镍的溶液中含有Ni2+和H2PO-2,在酸性等条件下发生下述反应:请配平Ni2++H2+PO-2→Ni++H2+PO-3.发布:2024/11/19 8:0:1组卷:5引用:1难度:0.5


