钛被誉为“现代金属”和“战略金属”。TiO2、TiSi、BaTiO3均为重要的钛的化合物。
(1)以高钛渣(主要成分为Ti3O5,含少量FeO、Fe2O3)为原料制备白色颜料TiO2的一种工艺流程如图:

①已知:Na2TiO3难溶于碱性溶液;H2TiO3中的杂质Fe2+,比Fe3+更易水洗除去。NaOH固体与Ti3O5在空气中加热至500~550℃时生成Na2TiO3,该反应的化学方程式为 2Ti3O5+O2+12NaOH 500-550℃ 6Na2TiO3+6H2O2Ti3O5+O2+12NaOH 500-550℃ 6Na2TiO3+6H2O。
②“酸溶”后获得的TiOSO4溶液经加热煮沸,生成难溶于水的H2TiO3,该反应的离子方程式为 TiO2++2H2O=H2TiO3↓+2H+TiO2++2H2O=H2TiO3↓+2H+。
③“脱色“时H2TiO3中因存在少量Fe(OH)3而影响TiO2产品的颜色,“脱色“步骤中Ti2(SO4)3的作用是 将Fe3+还原为Fe2+便于除去从而提高H2TiO3的纯度将Fe3+还原为Fe2+便于除去从而提高H2TiO3的纯度。
(2)在熔融盐体系中,通过电解TiO2和SiO2获得电池材料(TiSi),电解装置如图1.写出电极A的电极反应 TiO2+SiO2+8e-=TiSi+4O2-TiO2+SiO2+8e-=TiSi+4O2-。

(3)钛酸钡(BaTiO3)被誉为“电子陶瓷工业的支柱”,其晶体结构如图2,在答题卡上用“△”标出Ti4+的位置 
 。
。
(4)TiO2可以催化降解甲醛、苯等有害物质,具有去除效率高,且无二次污染等优点,广泛应用于家居装潢等领域,根据图推导X的化学式 HCO-3HCO-3,并描述步骤②、③的反应机理 羟基结合甲醛的氢产生H2O和醛基,醛基再与O-2结合产生HCO-3羟基结合甲醛的氢产生H2O和醛基,醛基再与O-2结合产生HCO-3。
500
-
550
℃
500
-
550
℃


HCO
-
3
HCO
-
3
O
-
2
HCO
-
3
O
-
2
HCO
-
3
【答案】2Ti3O5+O2+12NaOH 6Na2TiO3+6H2O;TiO2++2H2O=H2TiO3↓+2H+;将Fe3+还原为Fe2+便于除去从而提高H2TiO3的纯度;TiO2+SiO2+8e-=TiSi+4O2-; ;;羟基结合甲醛的氢产生H2O和醛基,醛基再与结合产生
;;羟基结合甲醛的氢产生H2O和醛基,醛基再与结合产生
500
-
550
℃
 ;
;HCO
-
3
O
-
2
HCO
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/10 0:0:4组卷:31引用:3难度:0.5
相似题
-
1.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如图:
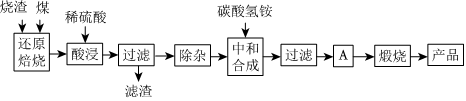
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,检验Fe3+已经除尽的试剂是;当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.
(5)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:114引用:4难度:0.5 -
2.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
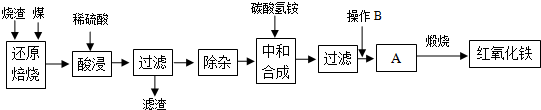
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,检验
Fe3+已经除尽的试剂是.
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是.
(5)煅烧A的反应方程式是.
(6)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:5引用:1难度:0.5 -
3.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
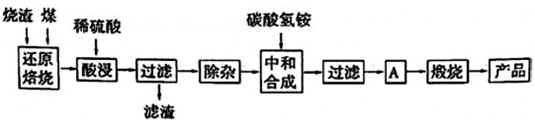
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常温下,当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.发布:2025/1/19 8:0:1组卷:12引用:1难度:0.5


