金属在人类生产中的应用十分广泛。
(1)三星堆遗址的Ⅱ号青铜神树引人注目,铸造铜树时,在铜中加入锡和铅会使材料的熔点 降低降低(选填“降低”、“升高”)。
(2)如图为锌与硫酸镍和硫酸锰混合溶液充分反应后粒子变化微观示意图。
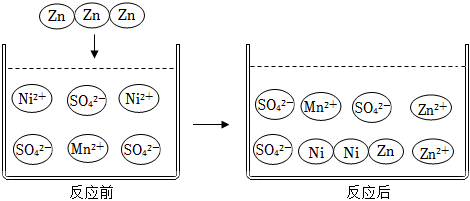
①Ni、Zn、Mn三种金属活动性由强到弱的顺序 Mn、Zn、NiMn、Zn、Ni。
②反应后溶液的质量会 增大增大(填“增大”或“减小”)。
(3)化学小组的同学收集到一些含硝酸银、硝酸铜的混合废液,同学们向其中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。则下列有关判断正确的是 DD(填字母)。
A.滤渣中一定有银,没有铜和锌
B.滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
(4)2022年全国钢铁产量高达10亿多万吨。铁的冶炼是化学研究的重要范畴。取12gFe2O3粉末,小组同学用如图装置模拟炼铁,并测定反应后固体的成分。
资料:CH4具有还原性,能与Fe2O3反应生成CO2、H2O和铁单质或铁的氧化物。
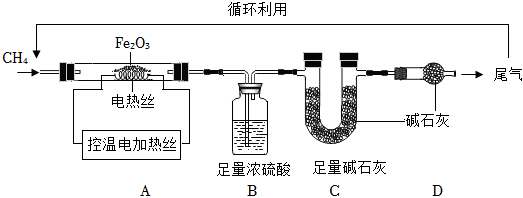
a.连接装置,先 检查装置气密性检查装置气密性,再装入药品
b.反应中循环使用CH4的目的是 充分利用资源充分利用资源。
c.若生成物充分被B、C装置吸收,B、C装置增加的质量比为 9:119:11。
d.控温加热一段时间后,继续通CH4至冷却,称得A中剩余固体为8.8g,若固体成分为Fe和FeO,则剩余固体中FeO的质量为 1.81.8g。
(5)2023年4月24日是第八个“中国航天日”。神舟十五号飞船成功发射,实现了“格物致知,叩问苍穹”的航空主题。
a.飞船进入太空后,白天太阳能电池板打开给电池充电,储存能量,夜间利用电池能量运行,电池在该过程中的能量转化形式为:太阳能→化学能化学能→电能。
b.飞船返回舱使用了钛合金等复合金属材料制成的“避火衣”,钛合金中的钛(Ti),一般用过量的镁在加热的条件下与TiCl4反应制得金属钛,发生反应的化学方程式为 TiCl4+2Mg △ 2MgCl2+TiTiCl4+2Mg △ 2MgCl2+Ti。
△
△
【答案】降低;Mn、Zn、Ni;增大;D;检查装置气密性;充分利用资源;9:11;1.8;化学能;TiCl4+2Mg 2MgCl2+Ti
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/21 8:0:9组卷:107引用:2难度:0.5


