由于机体缺乏铁元素,血红蛋白合成减少所导致的贫血称为缺铁性贫血。无机硫酸亚铁是常见的口服补铁剂,某实验小组进行了硫酸亚铁的制备及含量测定。
已知:①FeSO4易被空气中氧气氧化;
②Fe2(SO4)3溶液能与Fe发生反应生成FeSO4溶液;
③硫酸浓度过高时会与铁、铜等金属反应产生SO2;
(1)如图1为铁元素的“价类二维图”。

①图1中E点对应物质易在空气中转化成D点对应物质,原因:氢氧化亚铁化学性质不稳定,在空气中易被氧气氧化氢氧化亚铁化学性质不稳定,在空气中易被氧气氧化。
②写出铁粉与稀硫酸制备硫酸亚铁的基本反应类型是:置换反应置换反应。
③有部分铁屑已生锈,铁锈主要成分用化学式表示:Fe2O3Fe2O3,
在制备硫酸亚铁过程中不需要对铁锈进行处理,可能的原因(用化学方程式表示)是:Fe+Fe2(SO4)3=3FeSO4。Fe+Fe2(SO4)3=3FeSO4。。
(2)探究制备硫酸亚铁时硫酸浓度
某实验小组进行了探究制备硫酸亚铁时硫酸浓度:取10份1g铁粉分别装入10支试管中,向其中滴入含有等量的H2SO4,但质量分数不同的硫酸进行实验,探究合适的硫酸浓度。
①实验小组选择用“含有等量的H2SO4,但质量分数不同的硫酸”,而不是用“等体积质量分数不同的硫酸”的原因是:等体积质量分数不同的硫酸溶液中硫酸质量不相等等体积质量分数不同的硫酸溶液中硫酸质量不相等。
②实验小组在实验过程中发现不适宜用浓度较高的硫酸,可能的原因是:硫酸浓度过高时会与铁、铜等金属反应产生SO2硫酸浓度过高时会与铁、铜等金属反应产生SO2。
(3)从溶液中获得FeSO4•7H2O晶体
如图所示为硫酸亚铁在不同温度下的溶解度曲线,且在不同温度下得到的硫酸亚铁晶体是不同的。从溶液中获得FeSO4•7H2O晶体的方法:

在57℃减压减压(填“加压”“减压”)蒸发,浓缩至 饱和饱和、冷却结晶冷却结晶、过滤、洗涤、低温干燥。适宜的洗涤液是 DD。
A.洗洁精
B.热水
C.冰水
D.饱和硫酸亚铁溶液
(4)样品中硫酸亚铁的含量测定
准确称取制得的硫酸亚铁样品1.41g于锥形瓶中,加蒸馏水完全溶解,加入稀硫酸,滴加溶质质量分数为1.58%的高锰酸钾溶液,当恰好完全反应时,消耗高锰酸钾溶液的体积为10.00mL(该高锰酸钾溶液密度近似为1g/mL)。列式计算该样品中硫酸亚铁的含量(结果用百分数表示,保留一位小数)。已知:高锰酸钾与硫酸亚铁反应的化学方程式为10FeSO4+2KMnO4+8H2SO4═5Fe2(SO4)3+2MnSO4+K2SO4+8H2O(相对分子质量:FeSO4=152,KMnO4=158,FeSO4•7H2O=278)
【答案】氢氧化亚铁化学性质不稳定,在空气中易被氧气氧化;置换反应;Fe2O3;Fe+Fe2(SO4)3=3FeSO4。;等体积质量分数不同的硫酸溶液中硫酸质量不相等;硫酸浓度过高时会与铁、铜等金属反应产生SO2;减压;饱和;冷却结晶;D
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/8 8:0:9组卷:64引用:1难度:0.4
相似题
-
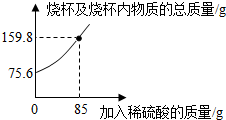 1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为g.
(2)计算样品中铁的质量分数(写出解题过程).发布:2025/1/9 8:0:2组卷:139引用:39难度:0.1 -
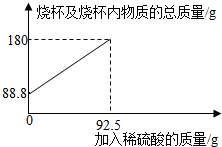 2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了10g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:4引用:1难度:0.3 -
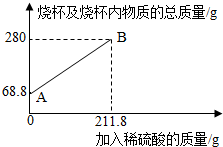 3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)求样品中铁的质量分数;反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了20g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:8引用:1难度:0.3


