当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:2114
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1555
更新:2025年05月26日
|
1121.工业上利用锌焙砂(主要成分为ZnO,含有少量CuO、As2O3、NiO等)生产高纯ZnO的流程示意图如图。
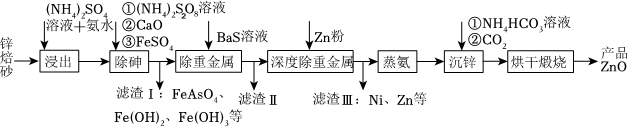
(1)用足量(NH4)2SO4溶液和氨水“浸出”锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是。
②通过“浸出”步骤,锌焙砂中的ZnO转化为[Zn(NH3)4]2+,该反应的离子方程式为。
(2)“浸出”时As2O3转化为。“除砷”步骤①中用(NH4)2S2O8作氧化剂,步骤①反应的离子方程式为AsO3-3。
(3)“除重金属”时,加入BaS溶液。滤渣Ⅱ中含有的主要物质是和BaSO4。
(4)“蒸氨”时会出现白色固体ZnSO4⋅Zn(OH)2,运用平衡移动原理解释原因:。
(5)“沉锌”步骤①中加入足量NH4HCO3溶液将白色固体转化为ZnCO3的离子方程式为。
(6)“煅烧”步骤中,不同温度下,ZnCO3分解的失重曲线和产品ZnO的比表面积变化情况如图1、图2所示。
已知:ⅰ.固体失重质量分数=×100%。样品起始质量-剩余固体质量样品起始质量
ⅱ.比表面积指单位质量固体所具有的总面积;比表面积越大,产品ZnO的活性越高。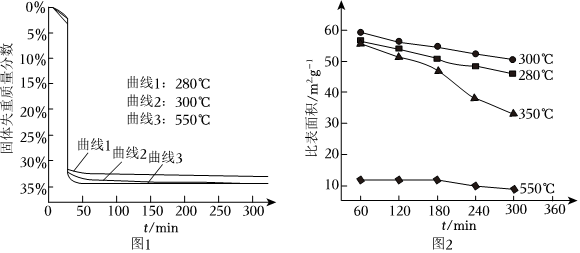
①280℃时煅烧ZnCO3,300min后固体失重质量分数为33.3%,则ZnCO3的分解率为%(保留到小数点后一位)。
②根据图1和图2,获得高产率(ZnCO3分解率>95%)、高活性(ZnO比表面积>40m2⋅g-1)产品ZnO的最佳条件是(填字母序号)。
a.恒温280℃,60~120min
b.恒温300℃,240~300min
c.恒温350℃,240~300min
d.恒温550℃,60~120min
(7)该流程中可循环利用的物质有。发布:2024/12/30 14:0:1组卷:94引用:5难度:0.51122.下列说法不正确的是( )
发布:2024/12/30 14:0:1组卷:24引用:6难度:0.81123.用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出。
(判断对错)发布:2024/12/30 14:0:1组卷:42引用:5难度:0.9 1124.观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
1124.观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
(1)属于离子结构示意图的是、(填编号).
(2)性质最稳定的原子是(填写编号,在本小题中下同),最容易失去电子的原子是,最容易得到电子的原子是.
(3)A、D两种元素形成的化合物在水溶液中的电离方程式.
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号、.发布:2024/12/30 14:0:1组卷:32引用:2难度:0.51125.氮化钡(Ba3N2)是一种重要的化学试剂。高温下,向氢化钡(BaH2)中通入氮气反应可制得氮化钡。已知:Ba3N2遇水反应;BaH2在潮湿空气中能自燃,遇水反应。用图4所示装置制备氮化钡时,下列说法正确的是( )
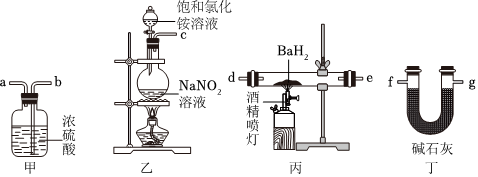 发布:2024/12/30 14:0:1组卷:61引用:3难度:0.6
发布:2024/12/30 14:0:1组卷:61引用:3难度:0.61126.新华社北京5月18日电,中共中央、国务院祝贺我国海域可燃冰试采成功.“可燃冰”又称“天然气水合物”,它是在海底的高压、低温条件下形成的,外观像冰.下面关于“可燃冰”的叙述不正确的是( )
发布:2024/12/30 14:0:1组卷:37引用:2难度:0.91127.如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
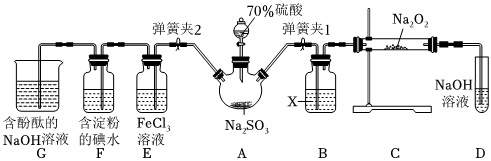
(1)在组装好装置后,若要检验A~D装置的气密性,其操作是首先,然后往D中装入水,然后微热A,观察到D中有气泡冒出,移开酒精灯或松开双手,D中导管有水柱形成且高度保持不变,说明装置气密性良好。
(2)装置D中盛放NaOH溶液的作用是。
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为;发生反应的离子方程式是。
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应。上述方案是否合理?(填“合理”或“不合理”),原因是。
(5)实验过程中G中含酚酞的NaOH溶液逐渐褪色,此实验证明SO2具有漂白性还是其溶于水显酸性?请设计实验验证:。发布:2024/12/30 14:0:1组卷:29引用:2难度:0.5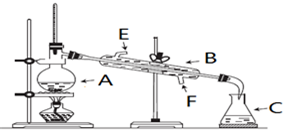 1128.如图是石油分馏实验装置,请回答:
1128.如图是石油分馏实验装置,请回答:
(1)写出仪器名称A:,B:;
(2)水银温度计的作用是;
(3)水流方向为从流入.发布:2024/12/30 14:0:1组卷:39引用:2难度:0.51129.关于裂解和裂化的叙述中,不正确的是( )
发布:2024/12/30 14:0:1组卷:28引用:2难度:0.7 1130.如图为元素周期表短周期的一部分,其中X元素原子最外层电子数是次外层的两倍。下列说法不正确的是( )发布:2024/12/30 14:0:1组卷:31引用:5难度:0.5
1130.如图为元素周期表短周期的一部分,其中X元素原子最外层电子数是次外层的两倍。下列说法不正确的是( )发布:2024/12/30 14:0:1组卷:31引用:5难度:0.5



