科学家在1925年发现了铼(Re)元素,由于铼可应用在高效能喷射引擎及火箭引擎,所以在军事战略上十分重要。NH4ReO4是制备高纯度Re的重要中间体。
Ⅰ.NH4ReO4的纯度测定
称取wgNH4ReO4样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1mol•L-1的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用c2mol•L-1NaOH标准溶液滴定过剩的HCl,达到终点时消耗V2mLNaOH溶液。
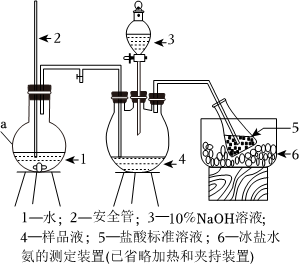
(1)仪器a是 圆底烧瓶圆底烧瓶(填名称)。
(2)冰盐水的作用是 防止氯化铵受热分解,使氨气逸出防止氯化铵受热分解,使氨气逸出。
(3)根据下表,滴定操作时宜选用 甲基红甲基红(填一种指示剂名称);滴定终点的现象是 滴入最后半滴NaOH溶液时,溶液由红色变为橙色,且半分钟内不变色滴入最后半滴NaOH溶液时,溶液由红色变为橙色,且半分钟内不变色。
部分指示剂变色的pH范围如下表:
| 指示剂名称 | 变色的pH范围 | 酸色 | 中性色 | 碱色 |
| 甲基红 | 4.4~6.2 | 红 | 橙 | 黄 |
| 酚酞 | 8.2~10.0 | 无 | 浅红 | 红 |
26
.
8
(
c
1
v
1
-
c
2
v
2
)
w
26
.
8
(
c
1
v
1
-
c
2
v
2
)
w
Ⅱ.高纯度铼的制取
从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉的流程如图:
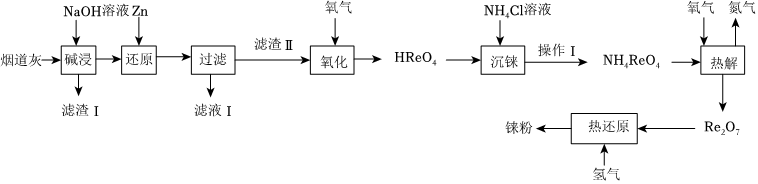
已知:过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(5)“碱浸”时Re2O7和MoO3与NaOH发生以下反应:Re2O7+2NaOH═2NaReO4+H2O;MoO3+2NaOH═Na2MoO4+H2O,则“滤渣Ⅰ”的成分为
CuO、Fe3O4
CuO、Fe3O4
。(6)“沉铼”时,加入热NH4Cl溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净的NH4ReO4晶体,“操作Ⅰ”包括
降温结晶
降温结晶
、过滤
过滤
、洗涤、干燥。(7)“热解”时,发生反应的化学方程式为
4NH4ReO4+3O2 2Re2O7+2N2+8H2O
热解
4NH4ReO4+3O2 2Re2O7+2N2+8H2O
。热解
【答案】圆底烧瓶;防止氯化铵受热分解,使氨气逸出;甲基红;滴入最后半滴NaOH溶液时,溶液由红色变为橙色,且半分钟内不变色;%;CuO、Fe3O4;降温结晶;过滤;4NH4ReO4+3O2 2Re2O7+2N2+8H2O
26
.
8
(
c
1
v
1
-
c
2
v
2
)
w
热解
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/7 8:0:9组卷:78引用:1难度:0.5
相似题
-
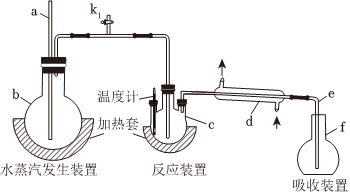 1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5
1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5 -
2.为探究矿石样品X(仅含两种元素)的组成和性质,某同学设计并完成如图实验:
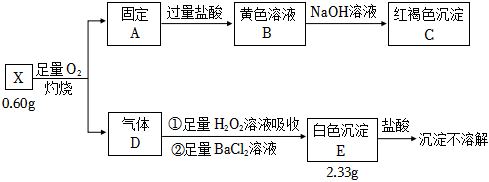
请回答:
(1)X含有的元素。
(2)X的化学式。
(3)红褐色沉淀C是。
(4)气体D通入足量H2O2中发生反应①的化学方程式。发布:2024/12/30 14:30:1组卷:16引用:3难度:0.7 -
3.煤气化是有效利用化石能源手段之一,有关反应如下:
①C+H2OCO+H2 ②CO+H2O高温CO2+H2一定条件
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
[实验]使水蒸气通过灼热的焦炭,收集反应后流出的气体。
[提出假设]对气体的成分提出了三种假设。
假设1:该气体是 CO、H2。
假设2:该气体是 CO、H2、H2O。
(1)假设3:。
[设计实验方案,验证假设]
他们拟用下图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)。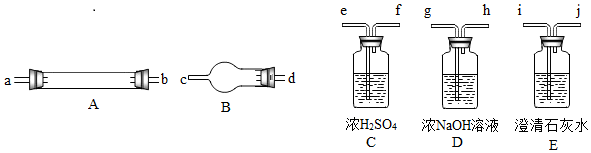
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):
混合气→dc→→→ij→→→→ij;
(3)仪器A中需加入试剂的是,其中反应的化学方程式是;
(4)仪器B中需加入试剂的名称是,其作用是;
[思考与交流]
(5)本实验的尾气需要处理,处理的方法为。
(6)某同学认为增加焦炭的量可以提高化学反应①的速率,你是否同意他的说法,并简述理由。发布:2024/12/30 14:0:1组卷:34引用:4难度:0.5
相关试卷


