某兴趣小组为验证质量守恒定律,做了红磷和镁条做燃烧的实验如图。

(1)观察到图1中的现象为 产生大量白烟,放出热量,气球膨胀,冷却后气球变得更瘪产生大量白烟,放出热量,气球膨胀,冷却后气球变得更瘪,红磷燃烧的符号表达式为 P+O2点燃P2O5P+O2点燃P2O5,小明认为根据质量守恒定律,燃烧前后的总质量应相等。待完全燃烧后,观察天平却往左边偏,出现此现象的原因是 反应后未塞紧瓶塞,外界空气进入锥形瓶反应后未塞紧瓶塞,外界空气进入锥形瓶。
小红按图2装置用适量镁粉进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
[提出问题]黄色固体是什么呢?
[查阅资料]①氧化镁为白色固体,难溶于水且不与水反应;②镁能与氮气反应只生成黄色的氮化镁Mg3N2固体;③氮化镁可与水反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑;④氢氧化镁是不溶于水的固体,且受热易分解生成氧化镁和水。
[做出猜想]黄色固体为 Mg3N2
[实验探究]
点燃
点燃
| 实验操作 | 实验现象及结论 |
如图,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B |
(2)现象: B中黄色固体溶解,有白色沉淀产生,并产生气泡,且A中溶液变为红色 B中黄色固体溶解,有白色沉淀产生,并产生气泡,且A中溶液变为红色 ;结论:燃烧产物含Mg3N2 |
(3)如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数
大于
大于
1
5
(4)请选择下列正确的实验方案将混在氧化镁中的氮化镁除去
D
D
。A.将混合物直接蒸馏
B.将混合物直接过滤
C.将混合物溶于水,待充分反应后过滤,再将滤渣在常温下干燥
D.将混合物放入水中,待充分反应后过滤,再将滤渣充分加热至固体质量不再变化
(5)空气中氮气的含量远大于氧气的含量,可是镁条在空气中的燃烧产物氧化镁却远多于氮化镁,合理的解释是
氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应
氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应
。(6)某可燃物质4.6克与9.6克氧气在密闭的容器里恰好完全燃烧,生成8.8克二氧化碳和5.4克水,问该可燃物由
碳、氢、氧
碳、氢、氧
元素组成,这些元素之间的质量比为 12:3:8
12:3:8
。【考点】质量守恒定律的实验探究.
【答案】产生大量白烟,放出热量,气球膨胀,冷却后气球变得更瘪;P+O2P2O5;反应后未塞紧瓶塞,外界空气进入锥形瓶;B中黄色固体溶解,有白色沉淀产生,并产生气泡,且A中溶液变为红色;大于;D;氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应;碳、氢、氧;12:3:8
点燃
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/23 4:0:1组卷:12引用:1难度:0.4
相似题
-
1.某学生为了探究甲烷的组成元素,设计并完成了如下探究实验,请你帮他完成下面的实验报告:
提出问题:甲烷中含有哪些元素?
【查阅资料】含碳元素的物质完全燃烧生成CO2。
实验探究:
(4)表达与交流:实验步骤 实验现象 解释与结论 ①在空气中点燃甲烷,
②将洁净干燥的小烧杯罩在甲烷燃烧的火焰上方。烧杯内壁有水珠。 (1)证明生成物有水,甲烷中一定含有 元素。③将蘸有澄清石灰水的小烧杯罩在甲烷燃烧的火焰上方。 (2) 。(3)证明生成物有CO2.甲烷中一定含有 元素。
经实验测定甲烷的化学式为CH4,请你写出甲烷燃烧方程式:。发布:2024/12/1 8:0:1组卷:6引用:1难度:0.5 -
2.某地农民将玉米秸秆等粉碎后放在密闭的沼气池内发酵制沼气,发酵后的残余物可做农家肥。我校化学兴趣小组的同学围绕“玉米秸秆主要由哪些元素组成”的问题展开了以下探究活动:
【猜想与假设】:根据沼气的成分猜想玉米秸秆中主要含有碳元素和氢元素。
【设计方案】:
【实验分析】:探究步骤 预计现象 相关结论 用坩埚钳夹持一小段烘干的玉米秸秆,点燃后伸入盛有氧气的集气瓶中 玉米秸秆剧烈燃烧,火焰熄灭后能够观察到瓶壁上有水珠 产物中有 向集气瓶中滴入少量 能够观察到 产物中有CO2
(1)将玉米秸秆烘干的目的是:。
(2)根据以上探究,同学们得出结论,秸秆中一定含有元素,可能含有元素(填元素符号)。发布:2024/11/19 8:0:1组卷:8引用:2难度:0.5 -
3.根据以下实验方案,“探究参加化学反应前后各物质的质量总和是否相等”,请将你的思考及实验结果写在短线处。
【猜想假设】:
(1)猜想1:相等;猜想2:。
【实验探究】
(2)
【反思评价】实验方案 方案一 方案二 实验装置 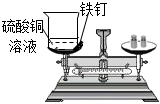
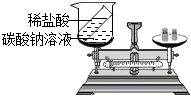
实验过程 分别将反应物及反应容器放在托盘天平上用砝码平衡 取下烧杯,将铁钉浸到硫酸铜溶液中,观察到的现象是 、溶液由蓝色逐渐变为浅绿色;再将其放回托盘天平,天平的指针(填“向左”或“向右”或“不”)偏转。取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯中,充分反应后再放回托盘天平,天平的指针 (填“向左”或“向右”或“不”)偏转,其原因是。
(3)你认为猜想是错误的,能用来验证质量守恒定律的反应需要满足的条件是。发布:2024/12/25 10:18:46组卷:12引用:2难度:0.5


