实验室以工业级硫酸锰粉末(含少量Ca、Co等的硫酸盐)为原料获得电池级MnSO4,并制备催化剂的载体Mn3O4。
(1)将工业级硫酸锰溶于水,蒸发结晶,趁热过滤除去部分杂质,过程中杂质去除率随MnSO4结晶率[m(结晶MnSO4)m(总MnSO4)×100%]的变化如图所示,杂质去除率随MnSO4结晶率的增大反而下降的原因是 水分大量蒸发,硫酸盐杂质结晶析出量增加水分大量蒸发,硫酸盐杂质结晶析出量增加。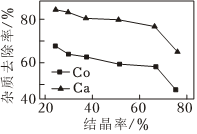
(2)将除去部分杂质的MnSO4溶于水,先后加入MnF2和MnS分别除去溶液中的Ca2+和Co2+,获得电池级硫酸锰。
①MnF2可将溶液中的Ca2+转化为CaF2,CaF2的晶胞如图所示,Ca2+周围距离最近且相等的F-个数为 88。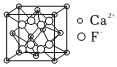
②“除钴”时,发生反应Co2++MnS(s)=CoS(s)+Mn2+,反应完全后,上层清液中c(Mn2+)c(Co2+)=10121012。[Ksp(MnS)=2×10-13,Ksp(CoS)=2×10-25]
(3)MnSO4溶液在碱性条件下通入空气氧化获得Mn3O4,产物中Mn元素质量分数(Mn%)随反应时间和温度变化如图1和图2所示。
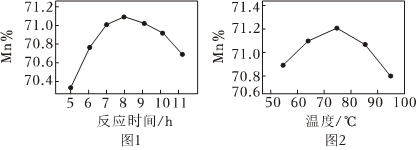
①如图1所示反应时间超过8小时,Mn%降低的原因是 MnSO4被氧化成更高价态锰的氧化物(Mn2O3或MnO2)MnSO4被氧化成更高价态锰的氧化物(Mn2O3或MnO2)。
②请设计由MnSO4溶液制备较纯Mn3O4实验方案:向MnSO4溶液中加入一定量1mol⋅L-1NaOH溶液,边搅拌边通入空气,控制75℃加热8h左右,过滤,洗涤,取最后一次洗涤滤液中加BaCl2溶液,无浑浊向MnSO4溶液中加入一定量1mol⋅L-1NaOH溶液,边搅拌边通入空气,控制75℃加热8h左右,过滤,洗涤,取最后一次洗涤滤液中加BaCl2溶液,无浑浊。(需用到的试剂:1mol⋅L-1NaOH溶液、BaCl2溶液)
m
(
结晶
M
n
S
O
4
)
m
(
总
M
n
S
O
4
)
c
(
M
n
2
+
)
c
(
C
o
2
+
)
【考点】晶胞的计算.
【答案】水分大量蒸发,硫酸盐杂质结晶析出量增加;8;1012;MnSO4被氧化成更高价态锰的氧化物(Mn2O3或MnO2);向MnSO4溶液中加入一定量1mol⋅L-1NaOH溶液,边搅拌边通入空气,控制75℃加热8h左右,过滤,洗涤,取最后一次洗涤滤液中加BaCl2溶液,无浑浊
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/10 8:0:8组卷:59引用:2难度:0.6
相似题
-
 1.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如下:
1.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如下:
①A的周期序数等于其主族序数;
②B、D原子的L层中都有两个未成对电子;
③E元素原子最外层电子排布式为(n+1)Sn(n+1)Pn-1;
④F原子有四个能层,K、L、M全充满,最外层只有一个电子.
试回答下列问题:
(1)基态E原子中,电子占据的最高能层符号为,F的价层电子排布式为.
(2)B、C、D的电负性由大到小的顺序为(用元素符号填写),C与A形成的分子CA3的VSEPR模型为.
(3)B和D分别与A形成的化合物的稳定性:BA4小于A2D,原因是.
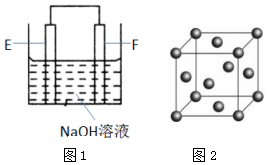
(4)以E、F的单质为电极,组成如图1所示的装置,E极的电极反应式为.
(5)向盛有F的硫酸盐FSO4的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色溶液,再向深蓝色透明溶液中加入乙醇,析出深蓝色晶体.蓝色沉淀溶解的离子方程式为.
(6)F的晶胞结构(面心立方)如图2所示:已知两个最近的F的距离为acm,F的密度为g/cm3(阿伏加德罗常数用NA表示,F的相对原子质量用M表示)发布:2025/1/18 8:0:1组卷:14引用:2难度:0.5 -
 2.铁及其化合物在生产生活及科学研究方面应用非常广泛。
2.铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为;其最外层电子的电子云形状为。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐
①NH4+电子式为。
②N、O两元素的第一电离能由大到小的顺序为(用元素符号表示)
③SO42-中S原子的杂化方式为,VSEPR模型名称为。
(3)K3[Fe(CN)6]晶体中中心原子的配位数为;晶体的配位体为(用化学符号表示)
(4)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为g•cm-3发布:2025/1/5 8:0:1组卷:7引用:1难度:0.7 -
 3.碳及其化合物有着重要用途。回答下列问题:
3.碳及其化合物有着重要用途。回答下列问题:
(1)基态碳原子的价层电子排布图为。
(2)在CH2=CHCN中,碳原子的杂化方式有、,所含σ键数目和π键数目之比为。
(3)甲烷、水、氨气中C、O、N原子均采用sp3杂化方式,VSEPR模型均为正四面体构型,比较三者键角的大小(由大到小,用H一R-H表示),其原因是。
(4)C60室温下为紫红色固体,不溶于水,能溶于四氯化碳等非极性溶剂。据此判断C60的晶体类型是。
(5)C60晶胞结构如图,C60分子处于顶点和面心。已知:C60晶胞棱长为14.20Å (1Å=10-8cm),则C60的晶体密度为g/cm3。
C60体中存在正四面体空隙(例如1、3、6、7四点构成)和正八面体空隙(例如3、6、7、8、9、12六点构成),则平均每一个C60晶胞中有个正四面体空隙和4个正八面体空隙。当碱金属元素全部占满所有空隙后,这类C60掺杂物才具有超导性。若用金属铯(Cs)填满所有空隙,距离最近的两个Cs原子间的距离为Å。发布:2025/1/5 8:0:1组卷:53引用:2难度:0.4


