元素周期表是化学中最重要的基本工具之一、它可以帮助化学家更好地研究元素,在科学研究和工业应用中有广泛应用。近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。
(1)比较离子半径:F-小于小于O2-(填“大于”“等于”或“小于”)。
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为 4f54f5。
(3)元素As与P同族,请举一事实说明非金属性P元素比As元素强 稳定性PH3>AsH3稳定性PH3>AsH3。
(4)已知H3PO4为三元酸,其结构式为: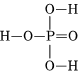 。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是
。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是 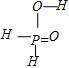
 。若将足量的KOH与次磷酸(H3PO2)充分反应,则化学方程式为 KOH+H3PO2=KH2PO2+H2OKOH+H3PO2=KH2PO2+H2O。
。若将足量的KOH与次磷酸(H3PO2)充分反应,则化学方程式为 KOH+H3PO2=KH2PO2+H2OKOH+H3PO2=KH2PO2+H2O。
(5)已知KH2PO4溶液呈酸性,可能的原因是 KH2PO4溶液电离程度大于其水解程度导致溶液显酸性KH2PO4溶液电离程度大于其水解程度导致溶液显酸性。


【答案】小于;4f5;稳定性PH3>AsH3; ;KOH+H3PO2=KH2PO2+H2O;KH2PO4溶液电离程度大于其水解程度导致溶液显酸性
;KOH+H3PO2=KH2PO2+H2O;KH2PO4溶液电离程度大于其水解程度导致溶液显酸性
 ;KOH+H3PO2=KH2PO2+H2O;KH2PO4溶液电离程度大于其水解程度导致溶液显酸性
;KOH+H3PO2=KH2PO2+H2O;KH2PO4溶液电离程度大于其水解程度导致溶液显酸性【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/11 1:0:1组卷:31引用:1难度:0.5
相似题
-
1.关于微粒半径大小的下列叙述中不正确的是( )
发布:2024/12/30 18:0:1组卷:16引用:2难度:0.6 -
2.( 1)比较离子半径:F-
(填“大于”“等于”或“小于”)O2-。
(2)Li+与H-具有相同的电子结构,r(Li+)小于r(H-),原因是。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),N、B、H三种元素电负性大小顺序是。
(4)光催化还原CO2制备CH4反应中,带状纳米 Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是。
(5)在周期表中,与Li的化学性质最相似的邻族元素是。
(6)下列状态的镁中,电离最外层一个电子所需能量最大的是(填字母)。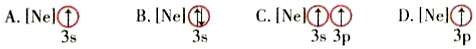
(7)黄铜是人类最早使用的合金之一,主要由Zn和 Cu组成。第一电离能I1(Zn)(填“大于”或“小于”)I1(Cu)。原因是。
(8)I1(Li)>I1(Na),原因是。I1(Be)>I1(B)>I1(Li),原因。
(9)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第2周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是;氮元素的E1呈现异常的原因是。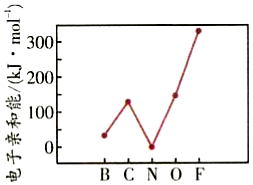 发布:2024/12/30 18:0:1组卷:21引用:2难度:0.3
发布:2024/12/30 18:0:1组卷:21引用:2难度:0.3 -
3.下列离子半径的大小顺序正确的是( )
①Na+
②X2-:1s22s22p63s23p6
③Y2-:2s22p6
④Z-:3s23p6发布:2024/12/30 18:30:1组卷:16引用:7难度:0.6


