恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g)2SO3(g)ΔH=-196.9kJ•mol-1]

(1)写出能表示硫的燃烧热的热化学方程式:S(s)+O2(g)═SO2(g)ΔH=-297kJ•mol-1S(s)+O2(g)═SO2(g)ΔH=-297kJ•mol-1.
(2)恒容条件下,下列措施中能使n(SO3)n(SO2)比图1所示情况增大的有 CC。
A.升高温度
B.充入He
C.再充入1molSO2(g)和1molO2(g)
D.使用催化剂
(3)恒温恒容时,1molSO2和2molO2充分反应,放出热量的数值比|ΔH2|大大(填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是 升高温度升高温度;图中表示平衡混合物中SO3的含量最高的一段时间是 t3~t4t3~t4。
n
(
S
O
3
)
n
(
S
O
2
)
【答案】S(s)+O2(g)═SO2(g)ΔH=-297kJ•mol-1;C;大;升高温度;t3~t4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/30 0:0:1组卷:3引用:1难度:0.7
相似题
-
1.在测定中和热的实验中,下列说法正确的是( )
发布:2024/12/18 23:0:1组卷:88引用:2难度:0.7 -
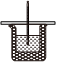 2.实验题:50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
2.实验题:50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃仪器是。
(2)写出表示该反应中和热的热化学方程式(中和热为57.3kJ•mol-1):(用离子方程式表示)。
(3)实验中改用60mL0.50mol•L-1盐酸与60mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求得的中和热(填“相等”或“不相等”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会(填“偏大””、“偏小””或“无影响”)。
(5)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差(t2~t1)分别为①3.3℃、②3.5℃、③4.5℃,则最终代入计算式的温差平均值为℃。计算该实验测得的中和反应反应热ΔH=(结果保留一位小数)[已知Q=cmΔt,设盐酸和NaOH溶液的密度为1g/cm3,反应后混合溶液的比热容(c)为4.18J/(g•℃)]。发布:2024/12/4 11:30:1组卷:60引用:3难度:0.6 -
3.掌握化学实验技能是进行科学探究的基本保证。下列有关说法正确的是( )
 发布:2024/12/17 3:0:1组卷:96引用:4难度:0.7
发布:2024/12/17 3:0:1组卷:96引用:4难度:0.7


