 某实验小组进行Na2SO3的有关探究活动
某实验小组进行Na2SO3的有关探究活动
Ⅰ.久置样品纯度的测定
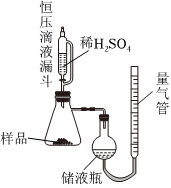
①按照如图(夹持装置已略)组装好装置,称量mg样品加入抽滤瓶,组装好装置;
②调节储液瓶与量气管的相对高度,让两边液面在同一水平线上,读数体积为V1mL;
③打开恒压滴液漏斗下端的活塞,加入过量的稀硫酸,让其充分反应;
④调节储液瓶与量气锌的相对高度,让两边液面在同一水平线上,读数体积为V2mL。
(1)进行实验前需进行的操作是 检查装置气密性检查装置气密性;
(2)使用恒压滴液漏斗添加稀硫酸的优点 使漏斗中的液体顺利流下,减小加入液体体积对测量气体体积的误差使漏斗中的液体顺利流下,减小加入液体体积对测量气体体积的误差;
(3)储液瓶中盛装的液体试剂是 饱和NaHSO3溶液饱和NaHSO3溶液,读数前要调节液面高度是为了消除 大气压强大气压强对气体体积影响;
(4)若该实验条件为标准状况,则Na2SO3纯度为 (V1-V2)×126×10-322.4m×100%(V1-V2)×126×10-322.4m×100%(用含V1、V2、m的式子表达,已知读数V1>V2);
Ⅱ.探究CuCl2溶液与Na2SO3溶液反应
将1mL0.2mol/LNa2SO3溶液与2mL0.2mol/LCuCl2溶液混合,立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有少量白色沉淀产生,振荡1min沉淀全部变为白色(CuCl)。
查阅资料:i橙黄色沉淀为2CuSO4•Cu2SO3•H2O,转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性;
ii原电池装置中物质氧化性与还原性强弱差异越大,电压越大。
(5)反应物生成白色沉淀的离子方程式为 SO2-3+2Cu2++2Cl-+H2O=2CuCl↓+SO2-4+2H+SO2-3+2Cu2++2Cl-+H2O=2CuCl↓+SO2-4+2H+,橙黄色沉淀与Cl-全部转化为CuCl的离子方程式 2CuSO4•Cu2SO3•H2O+6Cl-=6CuCl↓+4SO2-4+2H+2CuSO4•Cu2SO3•H2O+6Cl-=6CuCl↓+4SO2-4+2H+;
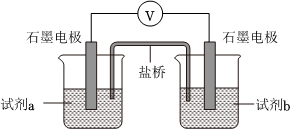
(6)设计如图实验装置,验证Cl-能提高Cu2+的氧化性:
(
V
1
-
V
2
)
×
126
×
10
-
3
22
.
4
m
×
100
%
(
V
1
-
V
2
)
×
126
×
10
-
3
22
.
4
m
×
100
%
SO
2
-
3
SO
2
-
4
SO
2
-
3
SO
2
-
4
SO
2
-
4
SO
2
-
4
| 试剂a | 试剂b | 电压表读数 |
| 0.2mol/LNa2SO3溶液 | 0.2mol/LCuCl2溶液 | E1 |
| 0.2mol/LNa2SO3溶液 | X | E2 |
0.2mol/LCuSO4溶液
0.2mol/LCuSO4溶液
,E1>
>
E2(填“>”、“<”或“=”)。【考点】探究物质的组成或测量物质的含量.
【答案】检查装置气密性;使漏斗中的液体顺利流下,减小加入液体体积对测量气体体积的误差;饱和NaHSO3溶液;大气压强;;+2Cu2++2Cl-+H2O=2CuCl↓++2H+;2CuSO4•Cu2SO3•H2O+6Cl-=6CuCl↓+4+2H+;0.2mol/LCuSO4溶液;>
(
V
1
-
V
2
)
×
126
×
10
-
3
22
.
4
m
×
100
%
SO
2
-
3
SO
2
-
4
SO
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/20 8:0:8组卷:20引用:1难度:0.5
相似题
-
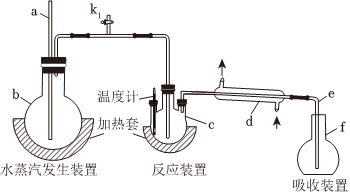 1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5
1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5 -
2.为探究矿石样品X(仅含两种元素)的组成和性质,某同学设计并完成如图实验:
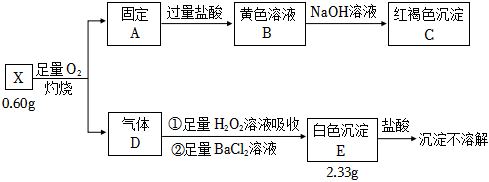
请回答:
(1)X含有的元素。
(2)X的化学式。
(3)红褐色沉淀C是。
(4)气体D通入足量H2O2中发生反应①的化学方程式。发布:2024/12/30 14:30:1组卷:16引用:3难度:0.7 -
3.煤气化是有效利用化石能源手段之一,有关反应如下:
①C+H2OCO+H2 ②CO+H2O高温CO2+H2一定条件
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
[实验]使水蒸气通过灼热的焦炭,收集反应后流出的气体。
[提出假设]对气体的成分提出了三种假设。
假设1:该气体是 CO、H2。
假设2:该气体是 CO、H2、H2O。
(1)假设3:。
[设计实验方案,验证假设]
他们拟用下图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)。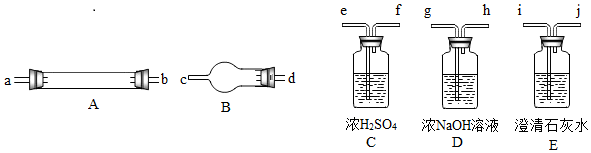
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):
混合气→dc→→→ij→→→→ij;
(3)仪器A中需加入试剂的是,其中反应的化学方程式是;
(4)仪器B中需加入试剂的名称是,其作用是;
[思考与交流]
(5)本实验的尾气需要处理,处理的方法为。
(6)某同学认为增加焦炭的量可以提高化学反应①的速率,你是否同意他的说法,并简述理由。发布:2024/12/30 14:0:1组卷:34引用:4难度:0.5


