【任务一】某小组研究Na2CO3和NaHCO3的性质,实验如下:
| 步骤 | 实验操作 | 观察到的实验现象 | |
| Na2CO3 | NaHCO3 | ||
| ① | 在两支试管中分别加入1.0gNa2CO3、1.0gNaHCO3固体,再加入5mL蒸馏水,振荡;将温度计分别插入其中 | 放置至室温时,全部溶解,得到透明溶液 | 放置至室温时,部分溶解,试管底部有少许固体 |
| ② | 将步骤①的试管中溶液分别分成两份,其中1份溶液中各滴加2滴酚酞溶液 | 溶液变红色 | 溶液变浅红色 |
| ③ | 在步骤②的另两份溶液中各滴加2滴10%盐酸,振荡 | 没有气泡产生 | 产生少量气泡 |
相同温度下,1gNa2CO3在5mL水中完全溶解,1gNaHCO3在5mL水中有少量固体残留
相同温度下,1gNa2CO3在5mL水中完全溶解,1gNaHCO3在5mL水中有少量固体残留
。(2)该实验
不能
不能
(填“能”或“不能”)说明Na2CO3溶液的碱性强于NaHCO3溶液,若不能,请说明理由 Na2CO3与NaHCO3的物质的量浓度不同,无法比较碱性强弱
Na2CO3与NaHCO3的物质的量浓度不同,无法比较碱性强弱
。(3)实验③中Na2CO3溶液没有气泡产生,学生甲得出结论:溶液与盐酸不反应。学生乙认为甲的结论不正确,支持学生乙观点的客观事实是
CO32-+H+=HCO3-
CO32-+H+=HCO3-
(用离子方程式说明)。【任务二】为进一步探究Na2CO3和NaHCO3的性质,利用传感器继续做如下实验:
| 编号 | 实验操作 | 实验数据 |
| ④ |
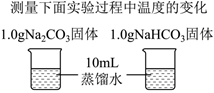
|
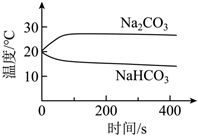
|
| ⑤ |
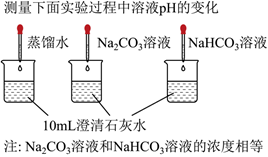
|

|
(4)实验④中,溶解时吸收热量的物质是
NaHCO3
NaHCO3
(填化学式)。(5)实验⑤中,Na2CO3溶液和澄清石灰水反应的离子方程式为
CO32-+Ca2+=CaCO3↓
CO32-+Ca2+=CaCO3↓
,OH-未参与该反应的实验证据是 加入Na2CO3溶液和加入蒸馏水的pH变化曲线相似
加入Na2CO3溶液和加入蒸馏水的pH变化曲线相似
。【任务三】探究NaHCO3和的热稳定性。
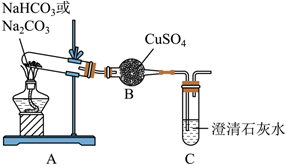
观察到的实验现象如下表所示:
| 物质 | 装置B中现象 | 装置C中现象 |
| Na2CO3 | 无明显变化 | 开始断断续续产生气泡,一会儿后,没有气泡,溶液保持澄清 |
| NaHCO3 | 白色粉末变蓝色 | 开始断断续续产生气泡,一会儿后,产生连续气泡,溶液变浑浊 |
(6)加热Na2CO3时,装置C中产生气泡的原因是
加热时排出了部分装置内空气
加热时排出了部分装置内空气
。(7)该实验所得结论是
Na2CO3的热稳定性比NaHCO3强
Na2CO3的热稳定性比NaHCO3强
。【考点】探究碳酸钠与碳酸氢钠的性质;性质实验方案的设计.
【答案】相同温度下,1gNa2CO3在5mL水中完全溶解,1gNaHCO3在5mL水中有少量固体残留;不能;Na2CO3与NaHCO3的物质的量浓度不同,无法比较碱性强弱;CO32-+H+=HCO3-;NaHCO3;CO32-+Ca2+=CaCO3↓;加入Na2CO3溶液和加入蒸馏水的pH变化曲线相似;加热时排出了部分装置内空气;Na2CO3的热稳定性比NaHCO3强
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/7 4:0:2组卷:36引用:2难度:0.6
相似题
-
1.某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中实验Ⅰ 实验Ⅱ 实验Ⅲ 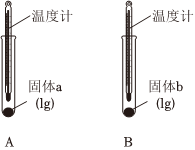
 (填“放出”或“吸收”)热量,可判断固体b为Na2CO3。
(填“放出”或“吸收”)热量,可判断固体b为Na2CO3。
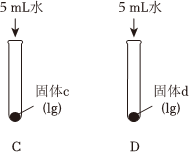
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。
①判断固体d为。
②分别向两支试管中滴加2滴酚酞,试管中红色较浅。
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因。
(4)请你再设计一个鉴别Na2CO3和NaHCO3的实验方案:。发布:2024/11/16 9:30:1组卷:93引用:2难度:0.7 -
2.Ⅰ.某小组同学进行Na2CO3和NaHCO3性质的探究,实验如下(夹持装置已略去,气密性已检验)。
(1)实验Ⅰ,能够证明Na2CO3的热稳定性强于NaHCO3的证据是实验Ⅰ 实验Ⅱ 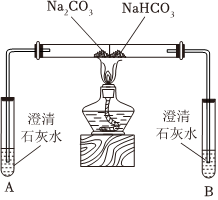
 。
。
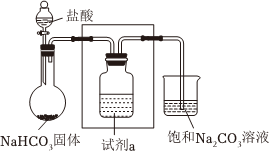
(2)实验Ⅱ,方框中为洗气装置,请将该装置补充完整。
(3)实验Ⅱ,试剂a为。
(4)实验Ⅱ,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:。
Ⅱ.实验小组继续利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱。
【实验过程】
【分析与解释】编号 实验操作 实验数据 实验Ⅰ 测量下述实验过程的温度变化 

实验Ⅱ 测量下述实验过程的pH变化 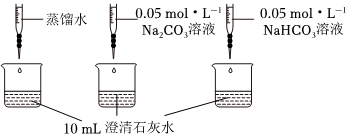
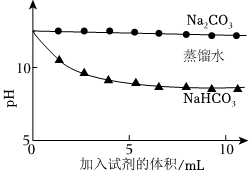
(1)实验Ⅰ中,溶解时吸收热量的物质是。
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式为,OH-未参与该反应的实验证据是。
(3)实验Ⅱ中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有。发布:2024/10/16 0:0:1组卷:21引用:1难度:0.7 -
3.国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)①若金属钠等活泼金属着火时,应该用来灭火。
②小苏打可治疗胃酸过多,其反应的离子反应方程式为:。
(2)火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S═K2S+N2↑+3CO2↑其中被氧化的元素是,还原产物是。
(3)人体内铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有(填“氧化性”或“还原性”)。
(4)探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,按如图装置图进行实验。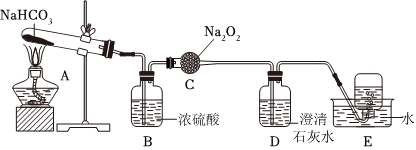
①C中反应的化学方程式为。
②E中收集的气体主要是。
(5)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个已配平的化学方程式。
▢ㅤㅤ+▢ㅤㅤ→▢ㅤㅤ+▢ㅤㅤ+▢ㅤㅤ+▢H2O发布:2024/10/12 11:0:2组卷:48引用:1难度:0.7


