Na2SO3、NaHSO3是常见的化工原料,常用作还原剂。
(1)25℃,H2SO3、HSO-3、SO2-3的物质的量分数[n(某微粒)n(H2SO3)+ n(HSO-3)+n(SO2-3)]与pH的关系如图所示。

①由表可知,NaHSO3溶液呈 酸酸性。(填“酸”或“碱”或“中性”)
②向NaOH溶液中通入SO2,所得溶液中一定存在的等式是 c(Na+)+c(H+)=c(OH-)+c(HSO-3)+2c(SO2-3)c(Na+)+c(H+)=c(OH-)+c(HSO-3)+2c(SO2-3)(用溶液中所含离子的物质的量浓度表示)。
③假设当c(H2SO3)=c(SO2-3)时,此时溶液pH=4.554.55。
(2)Na2SO3固体久置后会被氧化。为测定某久置Na2SO3固体中Na2SO3的含量,现进行如下实验:称取0.3000g该固体于锥形瓶中,加水溶解后,边振荡边向其中滴加0.1000mol•L-1I2标准溶液28.00mL,充分反应后向溶液中滴加2滴淀粉溶液作指示剂,继续滴加0.1000mol•L-1Na2S2O3标准溶液与过量的I2反应(发生反应I2+2Na2S2O3=2NaI+Na2S4O6),恰好完全反应时消耗Na2S2O3标准溶液16.00mL。
①滴定终点时的实验现象是 当滴入最后一滴硫代硫酸钠溶液时,溶液由蓝色变为无色,且半分钟内不恢复说明达到滴定终点当滴入最后一滴硫代硫酸钠溶液时,溶液由蓝色变为无色,且半分钟内不恢复说明达到滴定终点。
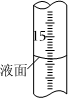
②滴定过程中,滴定管液面如图所示,此时滴定管的读数为 15.80mL15.80mL。
③计算久置Na2SO3固体中Na2SO3的百分含量 84%84%。
④下列情况会造成滴定或读取所滴Na2S2O3标准溶液体积偏大的是 BCBC(填序号)。
A.滴定过程中用蒸馏水冲洗锥形瓶瓶壁
B.装Na2S2O3标准溶液的滴定管水洗后未润洗
C.开始滴定时,滴定管尖嘴部分未充满液体
D.滴定前仰视读数,滴定后俯视读数
HSO
-
3
SO
2
-
3
n
(
某微粒
)
n
(
H
2
S
O
3
)
+
n
(
HS
O
-
3
)
+
n
(
S
O
2
-
3
)
HSO
-
3
SO
2
-
3
HSO
-
3
SO
2
-
3
SO
2
-
3
【考点】探究物质的组成或测量物质的含量;盐类水解的应用.
【答案】酸;c(Na+)+c(H+)=c(OH-)+c()+2c();4.55;当滴入最后一滴硫代硫酸钠溶液时,溶液由蓝色变为无色,且半分钟内不恢复说明达到滴定终点;15.80mL;84%;BC
HSO
-
3
SO
2
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/11 4:0:2组卷:6引用:1难度:0.6
相似题
-
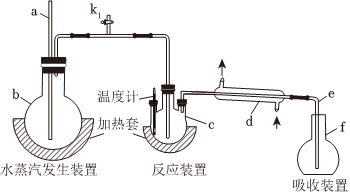 1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5
1.为测定某氟化稀土样品中氟元素的质量分数进行如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量,实验装置如图所示。(1)a的作用是 ,f仪器的名称是(2)检查装置气密性:首先(填操作),关闭k1,微热c,f中有气泡冒出;停止加热,导管e内形成一段稳定的水柱,说明装置气密性良好。(3)c中加入一定体积高氯酸和mg氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使水蒸气进入c。①下列物质可代替高氯酸的是(填序号)A.硝酸 B.盐酸 C.硫酸 D.磷酸②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成,若有SiF4生成,实验结果将(填“偏高”“偏低”或”不受影响”)。③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是。(4)向馏出液中加入V1mL c1 mol/L La(NO3)3溶液,得到LaF3沉淀,再用c2mol/L EDTA标准溶液滴定剩余的La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为。(F的相对原子质量为19)(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏实验),测量并计算出氟元素质量,重复多次。该操作的目的是。发布:2025/1/18 8:0:1组卷:24引用:1难度:0.5 -
2.煤气化是有效利用化石能源手段之一,有关反应如下:
①C+H2OCO+H2 ②CO+H2O高温CO2+H2一定条件
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
[实验]使水蒸气通过灼热的焦炭,收集反应后流出的气体。
[提出假设]对气体的成分提出了三种假设。
假设1:该气体是 CO、H2。
假设2:该气体是 CO、H2、H2O。
(1)假设3:。
[设计实验方案,验证假设]
他们拟用下图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)。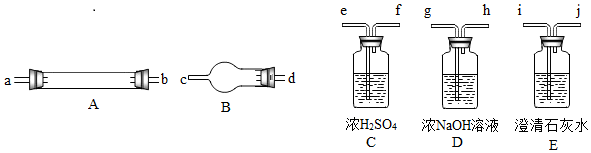
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):
混合气→dc→→→ij→→→→ij;
(3)仪器A中需加入试剂的是,其中反应的化学方程式是;
(4)仪器B中需加入试剂的名称是,其作用是;
[思考与交流]
(5)本实验的尾气需要处理,处理的方法为。
(6)某同学认为增加焦炭的量可以提高化学反应①的速率,你是否同意他的说法,并简述理由。发布:2024/12/30 14:0:1组卷:34引用:4难度:0.5 -
3.为探究矿石样品X(仅含两种元素)的组成和性质,某同学设计并完成如图实验:
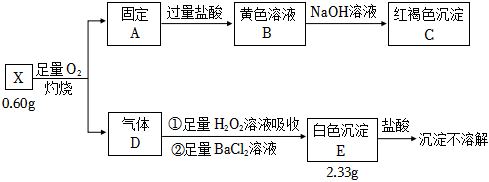
请回答:
(1)X含有的元素。
(2)X的化学式。
(3)红褐色沉淀C是。
(4)气体D通入足量H2O2中发生反应①的化学方程式。发布:2024/12/30 14:30:1组卷:16引用:3难度:0.7


